Theresia Gutmann
Funktionsweise des Insulinrezeptors in seiner Membranumgebung
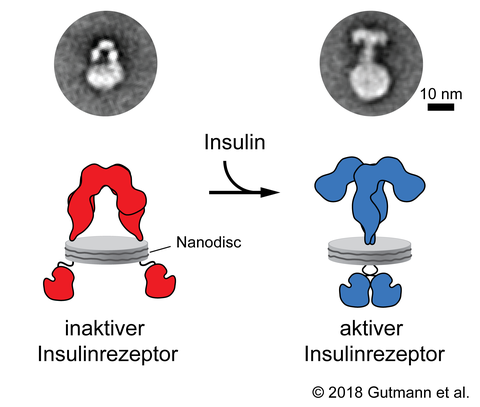
Unsere Zellen sind auf Insulin angewiesen, um Zucker effizient aus dem Blut aufnehmen zu können. Dazu muss es von außen an seinen Rezeptor, den sogenannten Insulinrezeptor, binden, welcher in der Zellmembran eingebettet ist. Wie der Insulinrezeptor schließlich durch Insulin genau aktiviert wird und wie dieses Signal durch die Membran ins Zellinnere übertragen wird, ist nicht vollständig verstanden.
Um molekulare Details der Insulinrezeptorbiologie untersuchen zu können, reinige ich humane Insulinrezeptoren in ihrer vollen Länge auf und rekonstituiere diese in synthetischen Membransystemen, um Details über ihren Aktivierungsmechanismus und den Einfluss ihrer Lipid-Umgebung zu analysieren. In enger Zusammenarbeit mit Prof. Thomas Walz von der Rockefeller University, USA, ist es uns erstmals gelungen, die durch Insulin induzierte strukturelle Änderung des intakten Rezeptors direkt zu visualisieren und damit ein Modell für den Mechanismus der Transmembransignalweiterleitung des Rezeptors zu postulieren (Gutmann et al., 2018; Short, 2018). Wir nutzen diese Daten als Grundlage für computergestützte Molekulardynamik (MD) Simulationen in Zusammenarbeit mit Prof. Ilpo Vattulainen (Universität Helsinki, Finnland) um diesen Aktivierungsprozess bei atomistischer Auflösung in Raum und Zeit verfolgen zu können.
Das Verständnis der Interaktion Insulins mit seinem Rezeptor auf molekularer Ebene ist von eminenter Bedeutung, um physiologische Prozesse verstehen und um gezielte Strategien zur Behandlung von Pathologien wie Diabetes zu entwickeln zu können.
Gutmann, T., K.H. Kim, M. Grzybek, T. Walz, and U. Coskun. 2018. Visualization of ligand-induced transmembrane signaling in the full-length human insulin receptor. J Cell Biol. [Epub ahead of print]
Short, B. 2018. Seeing the insulin receptor in action. The Journal of Cell Biology. [Epub ahead of print]