AG Antos
Meine Gruppe ist interessiert an Geweberegeneration, einschließlich kardialer Physiologie. Um die Biologie hinter der Geweberegeneration besser zu verstehen bin ich an der Beantwortung folgender fundamentaler Fragen interessiert:
1. Wie werden Zellen am Ort der Verletzung induziert um verlorenes Gewebe zu regenerieren.
2. Wie sind Zellen beteiligt, während der Regeneration kontrolliert die richtige Struktur zu produzieren.
3. Was hält die Regeneration an, sobald die adäquate Größe erreicht ist.
Um diese Fragen zu beantworten verwendet meine Arbeitsgruppe den Zebrafisch, da der Zebrafisch in der Lage ist Herz, Gliedmaßen, usw. komplett zu regenerieren. Somit können wir die Zelle und die zugrundeliegenden molekularen Mechanismen, welche an den Regenerationsfähigkeiten des Fisches beteiligt sind, beschreiben und im Detail betrachten.
Die Physiologie des gesunden Herzens benötigt einen geregelten Ca2+-Haushalt über den gesamten synzytialen Herzmuskel. Während Einzelzell-Experimente mit Kardiomyozyten in Kultur zeigen wie der einzelne Kardiomyozyt seine subzelluläre Ca2+-Verteilung und dessen Haushalt reguliert, können solche Versuche nicht die synzytiale Natur der Kardiomyoyzten im Herzen in vivo nachstellen. Daher werden hier experimentelle Präparationen der Organe benötigt, um bekannte (katecholaminerge und natriuretische Signale) und zurzeit noch unbekannte Mechanismen der Regulation der Herzphysiologie in vivo zu verstehen. Hierfür verwenden wir bildgebende Verfahren, um in vivo in Echtzeit das Zebrafisch-Herz darzustellen und so fundamentale Fragen der kardialen Kontraktilität, Verletzung und Regeneration zu beantworten.
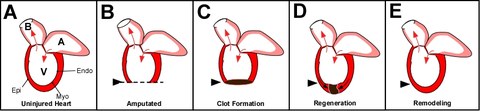
Bild 1: Zebrafischherz-Regeneration. A) Das adulte Zebrafischherz besteht aus einem Ventrikel (V), einem Atrium (A) und dem Balbus artieriosis (B). Die Pfeile zeigen die Richtung des Blutflusses. Ähnlich der Herzwand von Säugetieren, besitzt der Fisch ein Epikardium (Epi), Myokardium (Myo) und Endokardium (Endo). Der Unterschied im Herz von Säugetieren und dem des adulten Zebrafisches liegt in der Fähigkeit des Fischherzens bei Verletzungen zu regenerieren. Amputation der ventrikulären Wand (B) resultiert in der Bildung eines Blutpfropfens (C). Dieser Pfropfen, und das nachfolgende Narbengewebe, bilden später das neue Myokardium, Epikardium und Endokardium und ersetzen dann das Narbengewebe, (D) bis es regeneriert ist (E).
Untersuchung in welcher Weise Calcineurin in die Biologie der Regulation des proportionalen Wachstums integriert ist.
Dieser Forschungsschwerpunkt bedingt zwei Fragen: 1) was initiiert regenerative Überwüchse und 2) was beendet die Regeneration an der proportional richtigen Größe. Inhibierung der Calcineurin-Aktivität führt zu Flossen, die aufgrund einer erhöhten regenerativen Wachstumsrate über ihre natürliche Größe hinaus regenerieren. Die Rate der Regeneration ist an eine proximo-distale Position in den Gliedmaßen gekoppelt. Mein Labor konnte zeigen, dass die Inhibition von Calcineurin zu Flossen führt, die aufgrund einer konstanten proximalen Wachstumsrate über ihre natürliche Größe hinaus regenerieren (Fig. 3). Des Weiteren führt die Inhibition von Calcineurin in verletzten Flossen zu Überwüchsen1. Daher wird die Erforschung der Regulation von Ca2+ und Calcineurin, dem Mechanismus der Calcineurin reguliert und den Zellen in denen dies stattfindet zu einer nachfolgenden Hypothese-basierten Erforschung der zellulären und molekularen Beziehung zwischen der Lageinformation und dem proportionalen Wachstum auf der einen Seite, und der Förderung des koordinierten Überwachsens auf der anderen Seite führen.
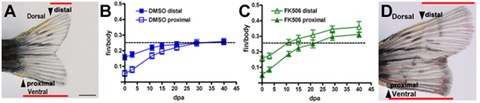
Bild 2: Calcineurin reguliert die positionsermittelnde Wachstumsrate. (A) Amputation eines Läppchens nach proximalem Schnitt (proximaler Pfeil) und einem distalen Schnitt (distaler Pfeil). (B) Der Graph zeigt die Beziehung der Wachstumsrate zwischen proximal und distal geschnittenen regenerierenden Läppchen in Relation zur Körperlänge und zeigt die Reduktion ihrer Raten, währen die Flosse zur originalen Größe der Läppchen regeneriert. (C) Inhibition von Calcineurin führt bei beiden regulierenden Läppchen zu einer konstanten proximalen Wachstumsrate, so dass diese weiterhin parallel wachsen können und über ihre originale Dimension hinaus wachsen. (D) Jedes Läppchen regeneriert mit derselben proximalen Rate nach Calcineurin-Inhibition, daher wachsen die Läppchen nicht zusammen [Nach Kujawski et al., 2014].
Quantitative Modellierung der in vivo Ca2+-Verteilungsmuster in spezifischen Geweben, der Region des Gewebes und der subzellulären Domäne während der Regeneration erlaubt es uns, mit Hilfe von konvokaler Mikroskopie zu untersuchen, wie Ca2+ Calcineurin reguliert um das allometrische Wachstum zu verhindern. Ich habe die Hypothese, dass das intrazelluläre Ca2+-Signal in Nanodomänen lokalisiert ist, in welchen das Calcineurin das Wachstum unterdrückt. Wir werden transgene Calciumreporter-Linien erstellen um diese Domäne zu identifizieren. Sobald wir diese identifiziert haben, besitzen wir die Möglichkeit diese Domäne mit den sie regulierenden Kanälen und Signalen zu verknüpfen. Dann können wir den Ort des Signals definieren und damit fortfahren den Ca2+-Calcineurin-verknüpften Mechanismus zu untersuchen, der das proportionale Wachstum reguliert. Da Ca2+ ein sekundärer Botenstoff für viele Enzyme ist, wird ein breiteres Verständnis der subzellulären Ca2+-Dynamik während der Geweberegeneration zu weiteren Möglichkeiten führen dessen potentielle Rolle in vivo in der Vorläuferzell-Bildung, bei Migration und Differenzierung, zusätzlich zur Wachstumsregulation, zu untersuchen. Außerdem verfolgen wir den Mechanismus der das Wachstum begünstigt, indem wir uns die beiderseitigen Kinase(n) genauer anschauen und durch Definierung des nachfolgenden Calcineurin-regulierten Mechanismus. Aus existierenden Zebrafisch-Varianten, der wissenschaftlichen Literatur und durch Deep Sequencing-Technologie, haben wir schon Ziele und Mechanismen für weitere Studien identifiziert: einen Kalium-Kanal, ein Connexin, Transkriptionsfaktoren, Wachstumsfaktoren und ein Chromatin-umbauendes Enzym. Des Weiteren bedeutet die Entdeckung, dass Arzneistoffe das regenerative Überwachsen verlängern können, dass wir ein Screening nach kleinen Molekülen und anderen Chemikalien durchführen können um Arzneistoff-Kandidaten und andere Komponenten des Mechanismus zu identifizieren, welche die proportionale Wachstumskontrolle regulieren und ein Hintergrund-Mutagenese-Screening für Flossenwachstums-Mutationen aufbauen können.
Untersuchung, wie Smp β-Catenin-abhängige Wnt-Signale reguliert und auf weitere Smp-Funktionen.
Meine Arbeitsgruppe identifizierte die Expression von simplet/fam53b (smp) in Vorläuferzellen des regenerierenden Herzens, Leber und Flossen durch bioinformatische Transkriptom-Analysen. Dieses Gen ist über eine Reihe von Vertebraten konserviert, aber seine Funktion war bisher unbekannt. Wir konnten zeigen, dass smp zur Regulation der Zellproliferation und der Strukturbildung des Gewebes während der Flossenregeneration benötigt wird. Daher wird mich die Untersuchung der Funktion von smp befähigen den Mechanismus des regenerativen Wachstums und der Strukturbildung besser zu verstehen.
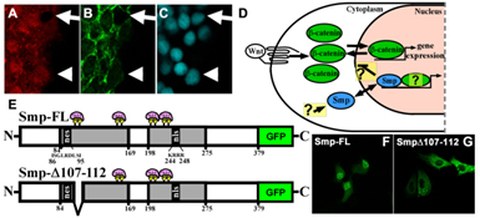
Bild 3: Smp wird benötigt für die β-Catenin-abhängige Wnt-Signalwirkung. (A) Immunohistochemische Färbungen für endogenes Smp, (B) für β-Catenin und (C) für DAPI. Der obige Pfeil zeigt die Abwesenheit von nukleärem Smp und β-Catenin an. Die Pfeilspitze darunter zeigt nukleäre Kolokalisation von Smp und β-Catenin. (D) Hypothetischer Mechanismus und Fragestellung wie Smp reguliert wird und wie es seinerseits β-Catenin und andere Partner reguliert. (E) Diagramm des Smp-Proteins welches die zwei konservierten homologen Regionen (HR) (grau), das nukleäre Lokalisationssignal in der zweiten (nls) und ein nukleäres Exportsignal (nes) in der ersten HR zeigt. (F) Smp ist vor allem im Zellkern und geringfügig im Zytoplasma lokalisiert. (G) Überexpression der Deletions-Mutante in (E) resultiert in kompletter zytoplasmatischer Lokalisation des Proteins.
In der Folge fand meine Arbeitsgruppe, dass Smp die nukleäre Lokalisation von β-Catenin reguliert, dass diese Regulation das nukleäre Lokalisationssignal im Smp-Protein benötigt, dass Smp β-Catenin reguliert indem es dieses im Zellkern hält und, dass dieses Protein in den Stamm- und Vorläuferzellen der Darmhöhlung von Säugetieren vorkommt, einer weiteren Seite der kanonischen Wnt-Signalwirkung. Die kanonische Wnt-Signalwirkung ist entscheidend für die Stammzell-Versorgung, die entwicklungsbiologische Strukturbildung, und die Geweberegeneration. Außerdem ist seine Regulation durch andere Signaltransduktionsmechanismen erforderlich für das kontrollierte Wachstum und die Strukturbildung des Gewebes. Unsere Entdeckung, dass Smp die nukleäre Lokalisation von β-Catenin reguliert, dass die nukleäre Lokalisation des Smp unabhängig von der Wnt-Signalwirkung ist1, außerdem das Anzeichen, dass Smp zwischen Cytoplasma und Zellkern transportiert wird, führt alles zu dem Schluss, dass Smp ein Regulationsknotenpunkt zwischen β-Catenin und anderen Signalmechanismen darstellt. (Fig. 2A-D). Zudem konnten wir kürzlich Sequenzen in Smp identifizieren, die den Zellkern-Cytoplasma-Transport regulieren. (Fig. 2E-G). Daher werden wir die Fragen beantworten, was reguliert die subzelluläre Verteilung von Smp, wie genau reguliert Smp die nukleäre Lokalisation des β-Catenins und ob Smp mit weiteren nukleären Proteinen interagiert um die Gen-Transkription β-Catenin-unabhängig zu regulieren. Um diese Fragen zu beantworten, werden wir mögliche β-Catenin-Regulatoren testen, andere Interaktionspartner durch Massenspektrometrie identifizieren und einschätzen wie post-translationale Modifikationen die subzelluläre Verteilung von Smp regulieren. Durch Messung des Echtzeit-Transports von Smp und β-Catenin in sich entwickelnden Zebrafisch-Embryos und regenerierenden Flossen und Messung der β-Catenin-Transkriptionsaktivität mittels transgener Zebrafisch-Reporterlinien, können wir die Dynamik der Regulation von β-Catenin während der Gewebsentwicklung und –regeneration abschätzen und modellieren. Durch die Identifizierung, wie andere Signalwege Smp regulieren, werden wir mehr über die post-transkriptionale Regulation von β-Catenin und anderen nukleären Faktoren erfahren. Einer davon ist 14-3-3. Somit werden meine Entdeckungen, aufgrund der Wichtigkeit der β-Catenin-abhängigen Signalwirkung, eine breitere Auswirkung im Forschungsfeld der Embryonalentwicklung und der Krebsforschung haben.