Klinische Elektrophysiologie des Herzens
Meine Arbeitsgruppe beschäftigt sich mit der Untersuchung der elektrischen Aktivität der Herzmuskelzelle bei Herzerkrankungen. Diese stellt die Grundlage für die am ganzen Herzen auftretenden elektrischen Signale dar, wie sie sich im Elektrokardiogramm darstellen lassen. Angeborene oder im Rahmen von Herzerkrankungen oder Vergiftungen erworbene Störungen der elektrischen Aktivität der einzelnen Herzmuskelzelle können zu Herzrhythmusstörungen und dem plötzlichen Herztod führen und sind damit für einen großen Anteil der durch Herzerkrankungen verursachten Todesfälle verantwortlich. Daher ist die Erforschung von Pathophysiologie und Pharmakologie der elektrischen Aktivität der Herzmuskelzelle von erheblicher medizinischer Bedeutung.
Die Themenschwerpunkte der Arbeitsgruppe umfassen den elektrischen und strukturellen Umbau des Herzens bei Herzhypertrophie und Herzinsuffizienz, die Regulation sowie die Pharmakologie kardialer Ionenkanäle.
Projekte
Der elektrische Umbau des Herzens bei Hypertrophie und Herzinsuffizienz
Herzhypertrophie führt zu einer Verlängerung der Aktionspotentialdauer im Arbeitsmyokard des Herzens und zur Entstehung von Nachdepolarisationen. Darüber hinaus trägt die hierdurch bedingte Störung der der Ordnung der Repolarisation zum Entstehen eines arrhythmogenen Substrates bei. Auf Ionenstromebene zeit sich der elektrische Umbau des Herzens in eine Verminderung von repolarisierenden K+ Strömen und einer Vergrößerung von depolarisierenden Strömen wie dem L-Typ Ca2+ Strom, dem schnellen Na+ Strom und insbesondere dem nicht inaktivierenden Anteil des Na+ Stromes. Ionenströme in einzelnen Kardiomyozyten können mit Hilfe der Patch-Clamp Technik (Abb. 1) gemessen werden.
Über die Veränderungen von Ionenströmen der Zellmembran hinaus kommt es zu Veränderungen im Ca2+ Haushalt der Kardiomyozyten, insbesondere von diastolischen Ca2+ Freisetzungen, die ebenfalls für die Entstehung von Nachpotentialen, Extrasystolen und Tachykardien verantwortlich sind. Den Ca2+ Haushalt von Kardiomyozyten untersuchen wir mit Hilfe von Epifluoreszenzmessungen, was das Aufzeichnen des Ca2+ Signals der Zelle und mit Hilfe von konfokaler Mikroskopie das Aufzeichnen von einzelnen diastolischen Ca2+ Freisetzungsereignissen erlaubt.
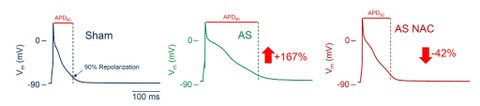
Wir konnten u.a. zeigen, dass oxidativer Stress eine bedeutende Rolle für die Verlängerung des Aktionspotentials und den Anstieg des L-Typ Ca2+ Stroms bei Drucküberlastung des Herzens spielt (Abb. 2).
Abb. 1: Isolierte Kardiomyozyte während der Untersuchung mittels Patch-Clamp Technik. Der Schatten ist die Patch-Pipette, die auf die Zelle aufgesetzt wird.
Abb. 2: Repräsentative Aktionspotentiale einer ventrikulären Kardiomyozyte einer aus einem scheinoperierten Herz (Sham), aus einem Herz mit durch Aorta ascendens Stenose induzierter Drucküberlastung (AS) und einem Herz mit Aorta ascendens Stenose unter Behandlung mit der anti-oxidativen Substanz N-Acetyl-Cystein. Die Zahlen geben die mittlere Veränderung der Aktionspotentialdauer (APD90) wieder.
Literatur:
Foltz, W. U.*, Wagner, M.*, Rudakova, E., Volk, T. (2012). N-acetylcysteine prevents electrical remodeling and attenuates cellular hypertrophy in epicardial myocytes of rats with ascending aortic stenosis. Basic Res Cardiol 107, 290.
Volk, T., Noble, P. J., Wagner, M., Noble, D., Ehmke, H. (2005). Ascending aortic stenosis selectively increases action potential-induced Ca2+ influx in epicardial myocytes of the rat left ventricle. Exp Physiol 90, 111-121.
Phosphodiesterase 2 als antiarrhythmisches Target
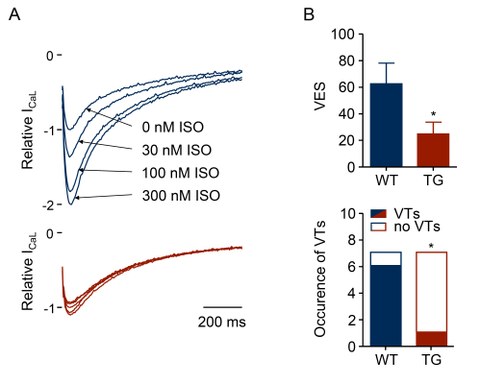
In letzter Zeit rückt mit der Phosphodiesterase 2 (PDE2) ein wichtiges und äußerst spannendes Enzym der β-adrenergen Signaltransduktion im Herzen in den Fokus meiner Arbeitsgruppe. Phosphodiesterasen bauen zyklische Nukleotide (cAMP, cGMP) ab und teilen damit die Zelle in Kompartimente auf, in denen cAMP bzw. cGMP vermittelte Signaltransduktion unabhängig von anderen Kompartimenten ablaufen kann. PDE2 nimmt hierbei eine Schlüsselrolle ein, da sie zum einen durch cGMP stimuliert wird, allerdings zum anderen hauptsächlich cAMP abbaut. Die PDE2 ist bei menschlichen Herzkrankheiten erhöht und spielt aller Wahrscheinlichkeit nach eine protektive Rolle, indem sie die protektive cGMP-abhängige Signaltransduktion mit der schädlichen cAMP abhängigen Signaltransduktion verbindet und diese hemmt. Im Tiermodell sorgt eine Überexpression der PDE2 für eine deutliche Protektion der Tiere von Arrhythmien (Abb. 3). Ziel unserer Arbeiten ist die Aufklärung der zugrundeliegenden zellulären Mechanismen und langfristig die therapeutische Nutzung im herzkranken Patienten.
Abb. 3: A, Stimulation des L-Typ Ca2+ Stromes durch Isoprenalin in einer Wildtyp Kardiomyozyte (oben) und einer Myozyte mit PDE2A3 Überexpression (unten). B, Reduktion der Anzahl von ventrikulären Extrasystolen (VES) und ventrikulären Tachykardien (VT) durch PDE2A3 Überexpression (TG).
Literatur:
Mehel, H., Emons, J., Vettel, C., Wittkopper, K., Seppelt, D., Dewenter, M., Lutz, S., Sossalla, S., Maier, L.S., Lechene, P., Leroy, J., Lefebvre, F., Varin, A., Eschenhagen, T., Nattel, S., Dobrev, D., Zimmermann, W.H., Nikolaev, V.O., Vandecasteele, G., Fischmeister, R., El-Armouche, A. (2013). Phosphodiesterase-2 is up-regulated in human failing hearts and blunts beta-adrenergic responses in cardiomyocytes. J Am CollCardiol 62, 1596-1606.
Regulation kardialer Ionenkanäle durch Steroidhormone
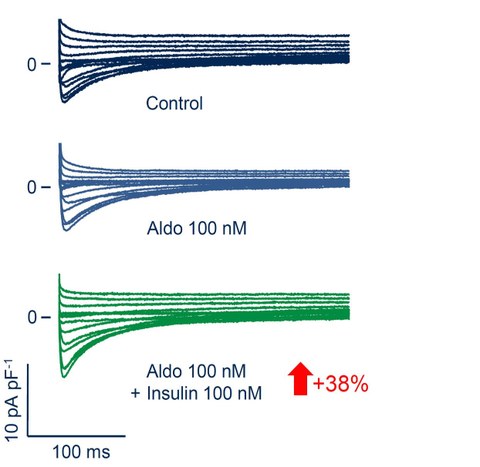
Seit der RALES Studie ist bekannt, dass die Aktivierung des kardialen Mineralocorticoidrezeptors (MR) eine wichtige Rolle in der Pathophysiologie der Herzinsuffizienz und des plötzlichen Herztodes spielt, da Patienten, die mit dem MR Antagonisten Spironolacton behandelt wurde eine deutlich verringerte Mortalität aufwiesen. Der Agonist und der Weg der Aktivierung des kardialen MR ist jedoch ein Rätsel, da bei der MR aufgrund der hohen Glucocorticoid Spiegel des Blutplasmas konstitutiv durch Glucocorticoide besetzt sein sollte und somit das als eigentlicher MR Agonist bekannte Aldosteron kaum eine Rolle spielen könnte. In Zellkultur an primären Kardiomyozyten konnten wir zeigen, dass Glucocorticoide über den MR zu einer Hochregulation des L-Typ Ca2+ Stromes führen. Darüber hinaus zeigt, wie erwartet, Aldosteron keinen zusätzlichen Effekt bei maximaler Aktivierung des MR mit Glucocorticoiden. Vor dem Hintergrund einer potentiell konstitutiven Aktivierung des kardialen MR durch Glucocorticoide konnten wir Insulin vermittelte Signaltransduktion über PI3-Kinase als einen für die MR vermittelte Hochregulation des L-Typ Ca2+ Stromes identifizieren.
Abb. 4: Aldosteron erhöht den kardialen L-Typ Ca2+ binnen 24h nur in Anwesenheit von Insulin, das selbst nach dieser Zeit keinen Effekt hat. Die Zahl neben dem Pfeil gibt den mittleren Effekt an.
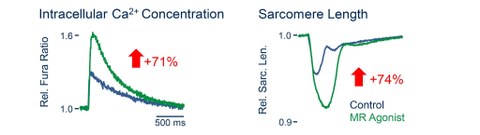
Abb. 5: Steigerung des intrazellulären Ca2+ Transienten (links) und der Kontraktilität (rechts) einer Kardiomyozyte nach 24 stündiger Inkubation mit dem MR und GR Agonist Dexamethason. Die Zahlen neben den Pfeilen geben den mittleren Effekt an.
Literatur:
Wagner, M., Moritz, A., Volk, T. (2011). Interaction of gonadal steroids and the glucocorticoid corticosterone in the regulation of the L-type Ca2+ current in rat left ventricular cardiomyocytes. Acta Physiol 202, 629-40.
Wagner, M., Rudakova, E., Volk, T. (2008). Aldosterone induced changes in cardiac ion channels are absent in rats on low salt diet and can be prevented by antioxidants in vitro. Pflugers Arch 457, 339-349.
Pharmakologie kardialer Ionenkanäle
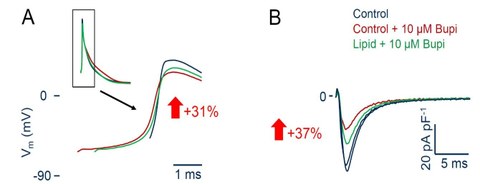
Insbesondere langwirksame, lipophile, Lokalanästhetika können bei systemischer Verabreichung zu starken neurologischen, aber auch kardiovaskulären Nebenwirkungen wie Blutdruckabfall, Herzrhythmusstörungen, Pumpversagen, Kammerflimmern und Asystolie mit potentiell tödlichem Ausgang führen. Aus diesem Grund ist die Entwicklung eines Gegenmittels als Behandlungsoption bei Lokalanästhetika Vergiftungen wünschenswert. In letzter Zeit mehren sich Fallberichte über die Wirksamkeit von Lipidemulsionen als Therapieoption (Lipid Rescue). Wir konnten auf Ebene der einzelnen Kardiomyozyten nachweisen, dass eine Lipidemulsion tatsächlich die Effekte des Lokalanästhetikums Bupivacain auf das kardiale Aktionspotential und den schnellen Na+ Strom antagonisieren kann und die Herabsetzung des freien Bupivacain Konzentration durch Adsorption an das Lipid als wichtigen Mechanismus der Wirkung demonstrieren.
Abb. 6: A, Bupivacain vermindert die Geschwindigkeit des Aufstrichs des Aktionspotentials (rot). Dies kann durch die Hinzugabe der Lipidemulsion (Lipovenös®) teilweise rückgängig gemacht werden (grün). B, auch der Effekt von Bupivacain auf den schnellen Na+ Strom (rot) kann teilweise durch die Lipidemulsion verhindert werden (grün). Die Zahlen neben den Pfeilen geben den mittleren Effekt der Lipidemulsion an.
Literatur:
Wagner, M., Zausig, Y. A., Ruf, S., Rudakova, E., Gruber, M., Graf, B. M., Volk, T. (2014). Lipid rescue reverses the bupivacaine-induced block of the fast Na+ current (INa) in cardiomyocytes of the rat left ventricle. Anesthesiology 120, 724-36.
Wagner, M., Riepe, K. G., Eberhardt, E., Volk, T. (2010). Open channel block of the fast transient outward K+ current by primaquine and chloroquine in rat left ventricular cardiomyocytes. Eur J Pharmacol 647, 13-20.
Methoden
Patch-Clamp Technik
Ca2+ Imaging
Echokardiographie
EKG Telemetrie