04.10.2018
Wie überleben Nervenzellen? Forschungsteam versucht den Zelltod zu stoppen

Dr. Volker Busskamp
Eine interdisziplinäre und internationale Forschergruppe um Dr. Volker Busskamp vom Zentrum für Regenerative Therapien Dresden der TU Dresden (CRTD) hat die Funktion eines kleinen nicht-kodierenden RNA-Moleküls, der so genannten miRNA, in der bisher höchsten Auflösung entschlüsselt. Diese Entschlüsselung der Genregulation ermöglicht Anwendungen zur Stärkung von Nervenzellen, um sie vor neurodegenerativen Erkrankungen zu schützen. Die hier verwendeten umfangreichen systembiologischen Methoden könnten zu einem neuen Standard für die Erforschung von miRNAs werden.
Die kleinen RNA-Moleküle wurden vor 25 Jahren entdeckt, aber noch weiß man wenig über ihren Einfluss auf die Genregulation von Boten-RNAs (mRNAs). Während computergestützte Studien die maximale Anzahl von miRNA-Interaktionen vorhersagen können, liefern experimentelle Studien in der Regel nur eine sehr kleine Anzahl von regulierten mRNAs. Das Forscherteam entdeckte, dass im Gegensatz zu früheren Annahmen die hirnspezifische miRNA (miR-124) während der neuronalen Entwicklung aus adulten menschlichen Stammzellen überflüssig ist, jedoch einen großen Einfluss auf das weitere neuronale Überleben hat.
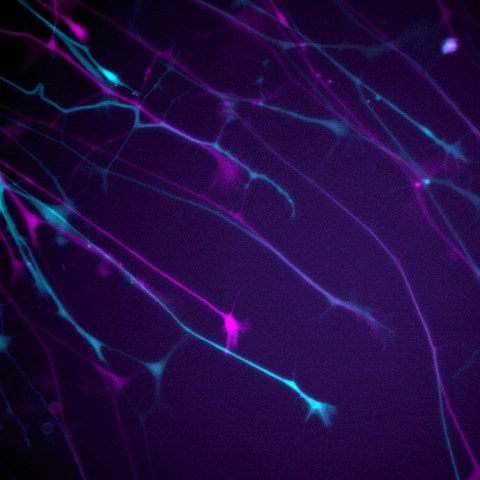
Neuritenwachstumsmessung von GFP-exprimierenden Neuronen. Der erste und letzte Zeitpunkt (0 min, 50 min) sind in Magenta und Cyan gezeigt.
Das Team kombinierte sowohl experimentelle als auch bioinformatische Ansätze und führte eine detaillierte Systemanalyse von miR-124 durch. Sie fanden 98 von miR-124 regulierte Gene, die gleichzeitig gesteuert wurden. Viele dieser kontrollierten Gene hatten direkte physiologische Funktionen, insbesondere den Schutz der Neuronen vor dem Absterben. Die Forschergruppe untersuchte mit einem neuartigen Berechnungsansatz auch indirekte Effekte, nämlich die miR-124-Zielgene, die selbst die Genexpression regulieren.
"Unsere tiefen Einblicke in die miRNA Regulation können zu neuen biomedizinischen Anwendungen führen, die den Schutz von Nervenzellen vor Degeneration ermöglichen. Zudem konnten bisher Gene mit unbekannten Eigenschaften in den regulatorischen Netzwerken untersucht und ihnen neue Funktionen zugewiesen werden", sagt Volker Busskamp. Der interdisziplinäre Ansatz der experimentellen Manipulation und der anspruchsvollen bioinformatischen Analyse setzt neue Maßstäbe in der miRNA-Genregulationsforschung.
Professor Katja Nowick (FU Berlin, Deutschland), Professor Johan Jakobsson (Universität Lund, Schweden), Professor Peter F. Stadler (Universität Leipzig, Deutschland) und Dr. Volker Busskamp (TU Dresden, Deutschland) sowie entsprechende Labormitglieder waren an diesem internationalen und interdisziplinären Projekt beteiligt.
Publikation
“Combined experimental and system-level analyses reveal the complex regulatory network of miR-124 during human neurogenesis”, Cell Systems DOI: 10.1016/j.cels.2018.08.011https://www.cell.com/cell-systems/fulltext/S2405-4712(18)30358-2
Webseite von Dr. Busskamp
http://www.crt-dresden.de/research/research-groups/core-groups/crtd-core-groups/neuronal-cell-types-and-circuit-engineering/
Volker Busskamp ist Freigeist-Fellow der VolkswagenStiftung und ERC Starting Grant Investigator.
Informationen für Journalisten:
Dr. Anka Kempe.
Tel.: +49 351 458 82060
Das 2006 gegründete Zentrum für Regenerative Therapien Dresden (CRTD) der Technischen Universität konnte sich in der zweiten Runde der Exzellenzinitiative erneut als Exzellenzcluster und DFG-Forschungszentrum durchsetzen. Ziel des CRTD ist es, das Selbstheilungspotential des Körpers zu erforschen und völlig neuartige, regenerative Therapien für bisher unheilbare Krankheiten zu entwickeln. Die Forschungsschwerpunkte des Zentrums konzentrieren sich auf Hämatologie und Immunologie, Diabetes, neurodegenerative Erkrankungen sowie Knochenregeneration. Zurzeit arbeiten acht Professoren und zwölf Forschungsgruppenleiter am CRTD, die in einem interdisziplinären Netzwerk von über 90 Mitgliedern sieben verschiedener Institutionen Dresdens eingebunden sind. Zusätzlich unterstützen 21 Partner aus der Wirtschaft das Netzwerk. Synergien im Netzwerk erlauben eine schnelle Übertragung von Ergebnissen aus der Grundlagenforschung in klinische Anwendungen. Das CRTD ist Teil des Center for Molecular and Cellular Bioengineering (CMCB).
