22.02.2018
Sächsisch-amerikanisches Forscherteam liefert neue Einblicke: So funktioniert der Insulinrezeptor

Dr. Ünal Coskun, , Gruppenleiter am PLID und Co-Seniorautor der Studie
Das Hormon Insulin steuert sowohl den Stoffwechsel als auch das Wachstum. Ist diese Funktion gestört, kann das zu schweren Krankheiten wie Diabetes mellitus oder Krebs führen. Die biologischen Wirkungen des Hormons werden durch ein passendes Protein auf der Zelloberfläche vermittelt – den sogenannten Insulinrezeptor.
In der aktuellen Studie konnten die Forschenden nun aufklären, wie der Rezeptor reagiert, sobald das Insulin an ihn an der Zelloberfläche bindet. Bisher war bekannt, dass Insulin von außen bindet und die Form des Proteins auf der Zellinnenseite sich daraufhin verändert, um das Signal weiterzugeben. Die Art der Strukturänderung blieb jedoch jahrzehntelang ein Rätsel, was dazu führte, dass widersprüchliche Modelle für die Aktivierung des Insulinrezeptors aufgestellt wurden.
“Um Einblicke in die Rezeptoraktivierung zu erhalten, haben wir vollständige, humane Insulinrezeptoren aufgereinigt und diese in sogenannte Nanodiscs eingebettet. Das sind wenige Nanometer große scheibenförmige Miniaturmembranen, welche dann direkt unter dem Elektronenmikroskop sichtbar gemacht werden konnten“, erklärt Doktorandin Theresia Gutmann, Co-Erstautorin der Studie. Sie arbeitet am Paul Langerhans Institut Dresden (PLID), welches zusammen vom Helmholtz Zentrum München mit dem Universitätsklinikum Carl Gustav Carus der Technischen Universität in Dresden betrieben wird.
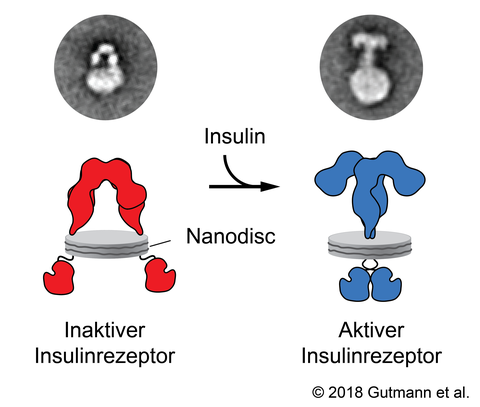
“Durch die Nanodisc-Technologie konnten wir also den Insulinrezeptor in einer künstlichen Membran direkt beobachten”, erklärt Dr. Ünal Coskun, Gruppenleiter am PLID und Co-Seniorautor der Studie. “In Abwesenheit von Insulin weist der Rezeptor die Gestalt eines umgekehrten “U” auf und hält so die beiden Enden voneinander getrennt. Allerdings müssen genau diesen beiden Enden – sogenannte Kinasedomänen – für die Signalweitergabe zusammengeführt werden.“ „Bindet nun aber das Insulin, erfolgt eine dramatische Reorganisation und der Rezeptor nimmt eine T-förmige Struktur an, wodurch sich die Kinasedomänen berühren und sehr wahrscheinlich die Signalübertragung auslösen“, führt Dr. Thomas Walz, Professor an der Rockefeller University, weiter aus.
Dr. Coskun ordnet die Studie ein: „Die in Nanodiscs eingebetteten Rezeptoren bieten eine vollkommen neue Möglichkeit, um weitere Fragen bezüglich der Insulinrezeptoraktivierung zu beantworten und potentiell therapeutische Wirkstoffe in definierten Umgebungen zu untersuchen.“ „Unsere Ergebnisse zeigen direkt die strukturellen Änderungen im vollständigen Rezeptor bei Insulinbindung und bieten eine Antwort auf die seit langem bestehende Frage nach dem Mechanismus, mit dem Insulin seinen Rezeptor aktiviert ”, so Co-Erstautorin Gutmann abschließend. Die Wissenschaftler aus Dresden sind Teil des Deutschen Zentrums für Diabetesforschung, kurz DZD.
Weitere Informationen
Original-Publikation:
Gutmann, Kim et al. (2018): Visualization of ligand-induced transmembrane signaling in the full-length human insulin receptor. Journal of Cell Biology, DOI: 10.1083/jcb.201711047
Das Paul Langerhans Institut Dresden (PLID) erforscht die Krankheitsursachen des Diabetes mellitus Typ 1, Typ 2 sowie des Schwangerschaftsdiabetes. Dabei sorgen zerstörte oder in ihrer Funktion eingeschränkte Betazellen für einen erhöhten Blutzuckerspiegel. Die Wissenschaftler des IPI/PLID arbeiten daran die Mechanismen zu entschlüsseln, die die Zerstörung und/oder Funktionseinschränkung der Betazellen bedingen und versuchen darüber hinaus neue Ansätze zu entwickeln um die geschädigten bzw. zerstörten Betazellen zu ersetzen. www.plid.de
Das Deutsche Zentrum für Diabetesforschung e.V. ist eines der sechs Deutschen Zentren der Gesundheitsforschung. Es bündelt Experten auf dem Gebiet der Diabetesforschung und verzahnt Grundlagenforschung, Epidemiologie und klinische Anwendung. Ziel des DZD ist es, über einen neuartigen, integrativen Forschungsansatz einen wesentlichen Beitrag zur erfolgreichen, maßgeschneiderten Prävention, Diagnose und Therapie des Diabetes mellitus zu leisten. Mitglieder des Verbunds sind das Helmholtz Zentrum München – Deutsches Forschungszentrum für Gesundheit und Umwelt, das Deutsche Diabetes-Zentrum DDZ in Düsseldorf, das Deutsche Institut für Ernährungsforschung DIfE in Potsdam-Rehbrücke, das Institut für Diabetesforschung und Metabolische Erkrankungen des Helmholtz Zentrum München an der Eberhard-Karls-Universität Tübingen und das Paul-Langerhans-Institut Dresden des Helmholtz Zentrum München am Universitätsklinikum Carl Gustav Carus der TU Dresden, assoziierte Partner an den Universitäten in Heidelberg, Köln, Leipzig, Lübeck und München sowie weitere Projektpartner. www.dzd-ev.de
Fachlicher Ansprechpartner und Ansprechpartner für die Medien:
Dr. Ünal Coskun, Paul Langerhans Institut Dresden des Helmholtz Zentrum München am Universitätsklinikum Carl Gustav Carus und der Medizinischen Fakultät der TU Dresden - Fetscherstrasse 74, 01307 Dresden - Tel. +49 351 796 5340 - E-Mail: