Kardiale Sheddomik
I. Die Funktion der Adam Metalloproteasen für die Entwicklung und Homöostase des murinen und humanen Myokards
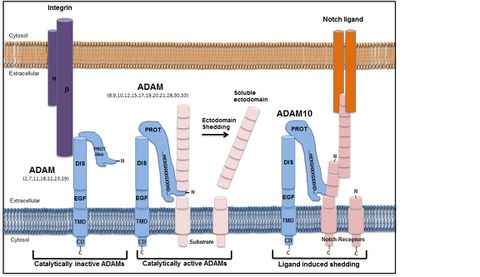
Die proteolytische Prozessierung von Membranproteinen wird auch als Ektodomänen Shedding bezeichnet. Die Familie der Zink-abhängigen Adam-Metalloproteasen stellt dabei eine der größten und physiologisch bedeutsamsten Klasen von Sheddasen dar. Adam-vermitteltes Ektodomänen Shedding konnte in einer Reihe von unterschiedlichen Geweben als essenzieller molekularer Vorgang für (embryonale) Zell-Differenzierung und adulte Zellhomöostase gezeigt werden (Abbildung 1). Die Bedeutung der Adam Metalloproteasen für Entwicklung und Homöostase des Myokards ist bis jetzt jedoch nur rudimentär untersucht worden.
Abb.1: Darstellung des Ektodomänen-Shedding Prozesses (aus Weber & Saftig 2012, Development)
Wir sind dabei diese Wissenslücke füllen und haben mittels Herzmuskelspezifischer ADAM10 knock-out Mäuse und Herzgewebeproben von Patienten mit unterschiedlichen kardiovaskulären Erkrankungen bereits die Erkenntnis gewonnen, dass ADAM10 Expression und Aktivität eine wichtige Rolle in der kardialen Homöostase einnimmt. Verschiedene mechanistische Studien und kardiale state-of-the-art Tiermodelle werden derzeit durchgeführt bzw. sind in Kürze geplant um die beobachteten Genotyp-Phänotyp Korrelation besser zu verstehen und ggf. in eine entsprechende Pharmakotherapie mit ADAM10-modulierenden Substanzen umzusetzen.
II. Adam Metalloproteasen als pharmakologische targets: „Refining status quo and looking beyond“
Aus einer Vielzahl an Studien konnte bis jetzt der übereinstimmende Konsens gefunden werden, dass die Aktivität der Metalloprotease ADAM10 eine wichtige Rolle bei embryonalen, degenerativen und regenerativen Prozessen in vitro und in vivo spielen. Molekular gesehen, wird dies in erster Linie durch Beeinflussung von
| a) | Zelldifferenzierung und/oder Proliferation über z.B. Notch//Wnt/β-catenin Signalgebung, |
| b) | interzellulärer Adhesion über z.B. Cadherine und Ephrin-Proteolyse |
| c) | Proteinaggregatbildung über z.B. veränderte Amyloid Precursor Protein (APP) oder Prion-Protein Proteolyse |
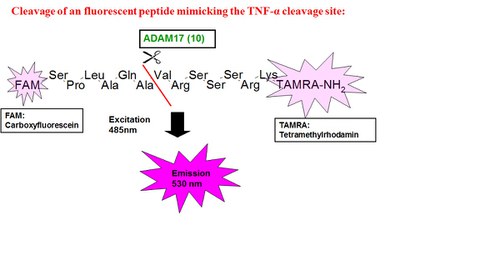
vermittelt. Da eine Fehlregulation dieser zentralen Signaltransduktionswege unweigerlich zu pathophysiologischen Effekten in Maus und Menschen führt, sollte ADAM10 ein bevorzugtes drug target sein. Aufgrund der frühen Letalität von konstitutiven sowie auch konditionalen ADAM10 knock-out Mäusen, sowie einer Reihe von enttäuschend verlaufenden klinischen Studie mit unspezifischen MMP/ADAM-Inhibitoren in den 90er Jahren wurde dieser Ansatz jedoch bis vor kurzem nicht konsequent verfolgt. Erste klinische Studie mit ADAM10-spezifischeren Substanzen, die entweder aktivierend aber auch inhibierende Wirkungen erzielten, zeigten jedoch keine offensichtlichen und/akuten Toxizitäten. Basierend auf diesen Erkenntnissen und mittels der Konzeptualisierung innovativer, neuer Ansätze (siehe z.B. Abb. 3) zur pharmakologischen Regulation von ADAM10 konnten wir sowohl Boehringer Ingelheim als auch Novartis als wichtige Partner bei der weiteren präklinischen Erforschung von ADAM10 als putativem drug target gewinnen.
Wir sind bereit überzeugt, dass ADAM10 ein wirkungsvoller Ansatzpunkt für die Bekämpfung einer Vielzahl von Erkrankungen ist. Jetzt liegt es an uns diese Erkenntnis in wirkungsvolle und nicht-toxische Therapieverfahren umzusetzen – darauf freuen wir uns!
Abb. 3: FRET-basierter Screening-Assays zur Identifikation neuartiger Wirkstoffe mit ADAM10/17 Aktivitätsregulierenden Eigenschaften
Wissenschafts-Intrapreneuring
Erfindungen und hieraus entstehende Innovationen sind die Triebfeder unserer Wissenschaft aber auch unserer Gesellschaft im Ganzen. Universitäten bieten aufgrund ihrer Ressourcenvielfalt an exzellent ausgebildeten Forschern und Administratoren, diverser Infrastruktur und abrufbarer Fördermittel bereits ein perfektes Umfeld, um diese komplexen Prozesse voranzutreiben. Dennoch gestaltet sich echte und nachhaltige Innovation in der Praxis häufig deutlich schwerer und ineffizienter als es die Ausgangslage vermuten lässt. Die Gründe hierfür sind vielfältig und nicht leicht zu beheben: Starre Karrierewege, Partikularinteressen, unflexible Förderungsmodalitäten sind nur einige wenige dieser Gründe. Trotzdem gelingen auch in unserem anspruchsvollen universitären Umfeld immer wieder herausragende Innovationen, die zeigen, dass es trotz aller Schwierigkeiten machbar ist.
Wie kommt es hierzu?
Meine persönlichen Erfahrungen und Beobachtungen aus mehr als 10 Jahren universitärer Forschungen haben gezeigt, dass es häufig einzelne Personen sind, die sich mutig über Widerstände hinweg setzen, Dogmen brechen, bereit sind quer zu denken und zu handeln aber auch in der Lage sind Menschen in einem schlagkräftigen Team zu sammeln und zu begeistern. Mit einem Wort: Unternehmer/Entrepreneure! Viele dieser Menschen verlassen unsere Universitäten leider viel zu früh, da sie entweder nicht in das bestehende Belohnungs- und Beförderungssystem passen oder weil sie sich entscheiden ihre Schaffenskraft in einem eigenen Unternehmen umzusetzen. Damit ist ihre Innovationskraft für die Universitäten und oft auch für unsere Gesellschaft, welcher die Universität als Einrichtung des öffentlichen Dienstes wie der Name schon sagt: dient – oft für immer verloren.
Ich glaube fest daran, dass wir diese Entwicklung stoppen können, wenn wir wissenschaftliches Unternehmertum innerhalb der Universitäten (Intrapreneurship) in Form von eigenen Karrierewegen und Fördermodalitäten unterstützen. Ich freue mich sehr, dass ich den Leiter des Integrativen Zentrums für Pharmakologie und Toxikologie (IZPT) Prof. Dr. Ali El-Armouche bereits für mein Herzensanliegen gewinnen konnte und nun als erster Wissenschafts-Intrapreneur für das IZPT wirken darf.
Sehen Sie sich selbst auch als Sponsor und/oder Wissenschafts-Intrapreneur? Dann freue ich mich darauf Sie persönlich kennen zu lernen, wenn sie mir eine Email an schicken.