29.08.2025
Fett-Mikroskopie: Lipide in Zellen sichtbar machen
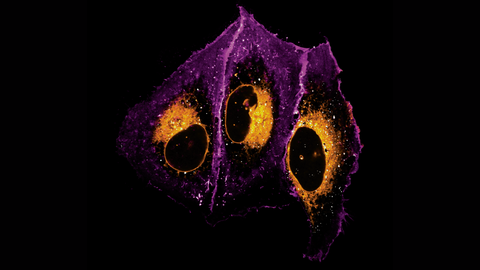
Mikroskopieaufnahme menschlicher Knochenzellen (U2OS). Das Lipid ist in orange erkennbar, die Zellmembran in lila und die Endosomen in weiß.
Lipidmoleküle, auch Fette genannt, sind für alle Lebensformen unverzichtbar. Sie sind aber mit Lichtmikroskopie nur schwer nachweisbar. Mit einer neuen chemischen Markierungsmethode hat ein Dresdner Team um André Nadler am Max-Planck-Institut für molekulare Zellbiologie und Genetik (MPI-CBG) und Alf Honigmann am Biotechnologischen Zentrum (BIOTEC) der TU Dresden diese Hürde überwunden und ermöglicht damit neue Einblicke. Die Forschenden konnten eine seit langem offene Frage beantworten: wie transportieren Zellen spezifische Lipide zu den Membranen ihrer Zielorganellen. Die neue Lipid-Bildgebungstechnik ermöglicht es, die Bedeutung des Lipidtransports bei gesunden und erkrankten Menschen besser zu verstehen.
Zellen benötigen Lipide, um Membranen aufzubauen, biochemische Reaktionen zu trennen und zu organisieren, Energie zu speichern und Informationen zu übermitteln. Jede Zelle kann Tausende verschiedener Lipide herstellen. Gerät dieses fein abgestimmte Gleichgewicht durcheinander, können Stoffwechsel- und neurodegenerative Erkrankungen entstehen. Noch immer ist nicht vollständig geklärt, wie Zellen die Vielzahl an Lipiden gezielt zwischen Organellen verteilen, um die Zusammensetzung jeder Membran aufrechtzuerhalten. Eine große Hürde dabei ist, dass Lipide schwer zu untersuchen sind, da bislang Mikroskopietechniken fehlten, mit denen sich ihre genaue Position in der Zelle verfolgen lässt.
Um dieses Problem zu lösen, entwickelten André Nadler, Chemiker und Biologe am Max-Planck-Institut für molekulare Zellbiologie und Genetik (MPI-CBG) in Dresden, und Alf Honigmann, Bioimaging-Spezialist am Biotechnologischen Zentrum (BIOTEC) der TU Dresden, in einer langjährigen Zusammenarbeit eine Methode, mit der Lipide in Zellen mithilfe herkömmlicher Fluoreszenzmikroskopie sichtbar gemacht werden können. Nach einer erfolgreichen Machbarkeitsstudie erweiterten sie das Team. Der Massenspektrometrie-Experte Andrej Shevchenko (MPI-CBG), Björn Drobot vom Helmholtz-Zentrum Dresden-Rossendorf (HZDR) und die Gruppe von Martin Hof vom J. Heyrovsky Institute of Physical Chemistry in Prag wurden Teil des Teams, um den Lipidtransport zwischen Zellorganellen genauer zu untersuchen.
Künstliche Lipide unter der Sonnenbank
„Wir begannen unser Projekt mit der Synthese einer Reihe minimal veränderter Lipide, die die wichtigsten Lipide in Organellenmembranen repräsentierten. Diese modifizierten Lipide unterscheiden sich nur durch wenige Atome von ihren natürlichen Gegenstücken, was uns ermöglichte, sie unter dem Mikroskop sichtbar zu machen und zu verfolgen“, erklärt Kristin Böhlig, Chemikerin und Doktorandin in der Nadler-Gruppe, die für die Lipidsynthese verantwortlich war.
Die modifizierten Lipide wurden in die Zellmembran lebender menschlicher Zellen geladen. Die Forschenden nutzten menschliche Knochen- oder Darmzellen in Zellkultur, da sie sich ideal für die Bildgebung eignen. Mit der Zeit wurden die Lipide in die Membranen der Organellen transportiert. Forschende konnten die modifizierten Lipide mit UV-Licht aktivieren, sodass sie an nahegelegene Proteine binden. Dies Vorgang stoppte ihren Transport innerhalb der Zelle.
„Nach der UV-Behandlung konnten wir die Lipide mithilfe der Fluoreszenzmikroskopie verfolgen und ihre Positionen über die Zeit dokumentieren. So erhielten wir ein umfassendes Bild des Lipidaustauschs zwischen Zellmembran und Organellenmembranen“, fasst Kristin Böhlig zusammen.
Um die Mikroskopiedaten zu verstehen, benötigte das Team eine maßgeschneiderte Bildanalyse-Pipeline. „“Für unsere speziellen Anforderungen habe ich einen Workflow mit automatisierter Bildsegmentierung entwickelt, die durch künstliche Intelligenz unterstützt wird. Damit lassen sich die Lipidströme durch das Zellorganellensystem quantifizieren“, erklärt Juan Iglesias-Artola, der die Bildanalyse durchgeführt hat.
Schneller Lipidtransport durch Proteine
Das Team kombinierte Bildanalyse mit mathematischer Modellierung, die von Björn Drobot am HZDR durchgeführt wurde. Die Ergebnisse zeigten deutlich: 85–95 % des Lipidtransports zwischen Organellenmembranen übernehmen Carrier-Proteine und nicht Vesikel. Dieser Transport außerhalb von Vesikeln ist viel spezifischer in Bezug auf einzelne Lipidarten und deren Sortierung in die verschiedenen Organellen der Zelle. Die Forschenden fanden außerdem heraus, dass der Lipidtransport durch Proteine zehnmal schneller erfolgt als durch Vesikel. Diese Ergebnisse legen nahe, dass die Membranzusammensetzungen der Organellen überwiegend durch schnellen, selektiven Proteintransport erhalten werden.
Parallel dazu untersuchte die Gruppe von Andrej Shevchenko am MPI-CBG mithilfe ultrahochauflösender Massenspektrometrie, wie sich Lipidstrukturen während des Transports von der Zellmembran zu den Organellen verändern.
Impulse für Lipide in Zellbiologie und Medizin
Dieser neue Ansatz ermöglicht es erstmals, quantitativ darzustellen, wie sich Lipide durch die Zelle zu verschiedenen Organellen bewegen. Die Ergebnisse lassen darauf schließen, dass der Transport von Lipiden außerhalb von Vesikeln eine wichtige Rolle bei der Aufrechterhaltung der Membranzusammensetzung einzelner Organellen spielt.
„Unsere Lipid-Bildgebungstechnik ermöglicht erstmals die mechanistische Analyse des Lipidtransports und der Lipidfunktionen direkt in Zellen“, erklärt Alf Honigmann, Professor für Biophysik an der TU Dresden und Forschungsgruppenleiter am BIOTEC. „Wir glauben, dass unsere Methode eine neue Ära in der Erforschung der Rolle von Lipiden in der Zelle einleitet.“
Die Technik könnte künftig helfen, die molekularen Grundlagen von Krankheiten zu verstehen, die durch Lipid-Ungleichgewichte entstehen und neue therapeutische Ansätze zu entwickeln, für lipidbedingte Erkrankungen wie die nicht-alkoholische Fettleber.
„Wir wussten, dass wir auf etwas Großes gestoßen waren.“
Projektleiter André Nadler erinnert sich: „Lipide in Zellen sichtbar zu machen, war immer eine der größten Herausforderungen der Mikroskopie. Unser Projekt war da nicht anders. Alf Honigmann und ich begannen, über die Lösung des Problems der Lipidbildgebung zu sprechen, sobald wir 2014/15 kurz nacheinander am MPI-CBG anfingen, und entschieden uns, es anzugehen. Fast fünf Jahre dauerte es, bis wir im Herbst 2019 endlich eine Probe mit einer klaren Zellmembranfärbung erhielten. Da wussten wir, dass wir auf etwas Großes gestoßen waren. Einige Monate später mussten wir jedoch aufgrund bestimmter weltbekannter Ereignisse unsere Labore schließen. Am Ende war diese Verzögerung sogar ein Vorteil. Erst durch die Revolution in der KI-gestützten Bildsegmentierung konnten wir die Daten wirklich quantifizieren, ohne sie wären unsere Aussagen deutlich eingeschränkter geblieben.“
Künftig wollen die Forschenden klären, welche Lipid-Transfer-Proteine für den selektiven Transport einzelner Lipidspezies verantwortlich sind und welche Energiequellen die gerichteten Lipidflüsse antreiben, die verhindern, dass die Membranzusammensetzungen der Organellen ins Gleichgewicht geraten.
Originalveröffentlichung
Juan M. Iglesias-Artola, Kristin Böhlig, Kai Schuhmann, Katelyn C. Cook, H. Mathilda Lennartz, Milena Schuhmacher, Pavel Barahtjan, Cristina Jiménez López, Radek Šachl, Vannuruswamy Garikapati, Karina Pombo-Garcia, Annett Lohmann, Petra Riegerová, Martin Hof, Björn Drobot, Andrej Shevchenko, Alf Honigmann und André Nadler: Quantitative imaging of lipid transport in mammalian cells. Naturel (August 2025)
Link: https://doi.org/10.1038/s41586-025-09432-x
Über das MPI-CBG
Das Max-Planck-Institut für molekulare Zellbiologie und Genetik (MPI-CBG) ist eines von über 80 Instituten der Max-Planck-Gesellschaft, einer unabhängigen gemeinnützigen Organisation in Deutschland. 600 Menschen aus 50 Ländern aus den verschiedensten Disziplinen arbeiten am MPI-CBG und lassen sich von ihrem Forscherdrang antreiben, um die Frage zu klären: Wie organisieren sich Zellen zu Geweben? Die Forschung des MPI-CBG deckt dabei eine möglichst weite Spanne an verschiedenen Komplexitätsstufen ab: auf der Stufe von molekularen Netzwerken, von Zellorganellen, von Zellen, von Gewebe, Organen oder auch auf mit Blick auf ganze Organismen. www.mpi-cbg.de
Über das BIOTEC
Das Biotechnologische Zentrum (BIOTEC) wurde 2000 als zentrale wissenschaftliche Einrichtung der TU Dresden mit dem Ziel gegründet, modernste Forschungsansätze in der Molekular- und Zellbiologie mit den in Dresden traditionell starken Ingenieurwissenschaften zu verbinden. Seit 2016 ist das BIOTEC eines von drei Instituten der zentralen wissenschaftlichen Einrichtung Center for Molecular and Cellular Bioengineering (CMCB) der TU Dresden. Das BIOTEC nimmt eine zentrale Position in Forschung und Lehre im Forschungsschwerpunkt Molecular Bioengineering ein und verbindet zellbiologische, biophysikalische und bioinformatische Ansätze miteinander. Es trägt damit entscheidend zur Profilierung der TU Dresden im Bereich Gesundheitswissenschaften, Biomedizin und Bioengineering bei.
www.tu-dresden.de/cmcb/biotec
www.tu-dresden.de/cmcb
Medienkontakt MPI-CBG:
Katrin Boes
Tel.: +49 351 210 2080
E-mail:
Medienkontakt BIOTEC:
Dr. Magdalena Gonciarz
Tel.: +49 351 458 82065
E-mail:
