Dec 01, 2017
Netzwerk Europäischer Wissenschaftler entdeckt neue Gene, die mit dem Ausfall insulinproduzierender Zellen bei Diabetes in Verbindung stehen
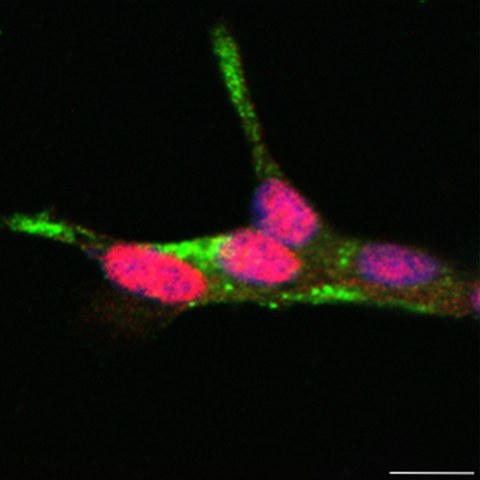
Validierung von PDX1, einem Transkriptionsfaktor der sich oberhalb der T2D-Inselsignaturgene befindet. Co-Immunofärbung für Insulin (grün) und PDX1 (rot) in humanen EndoC-βH1 Zellen. Zellkerne sind mit DAPI (blau) gegengefärbt.
TUD, imidia, efpi und imi - Pressemitteilung hier zum Download.
Unterstützt von Wissenschaftlern der Hochschulmedizin der TU Dresden ist es gelungen, fehlregulierte Gene in der Bauchspeicheldrüse zu finden, die bei vielen Typ-2-Diabetes Patienten immer wieder auftauchen. English and Italian version below.
Dresden, Frankfurt, Germany / Lausanne, Schweiz / Pisa, Italien
Typ-2-Diabetes, der weltweit rund eine halbe Milliarden Menschen betrifft, resultiert aus der Unfähigkeit der Betazellen der Bauchspeicheldrüse, dem Körper ausreichend Insulin zuzuführen, um den Blutzuckerspiegel für ein gesundes Leben aufrechtzuerhalten. Unter der Leitung von Prof. Michele Solimena an der Technischen Universität Dresden und des Helmholtz Zentrum München, Dr. Anke M Schulte von Sanofi in Frankfurt, Dr. Mark Ibberson vom Schweizer Institut für Bioinformatik (Lausanne) und Prof. Piero Marchetti von der Universität von Pisa und als Teil des EU-Innovative Medicine Initiative (IMI) Forschungskonsortiums IMIDIA, haben die Wissenschaftler in einer gemeinsamen Studie einen neuartigen Cluster von fehlregulierten Genen in den Pankreasinseln von Patienten mit Typ-2-Diabetes identifiziert. Diese Erkenntnisse wurden nun in Diabetologia veröffentlicht, der Fachzeitschrift der European Association fort he Study of Diabetes (EASD).
„Wir glauben, dass unsere Daten neue molekulare Erkenntnisse darüber liefern, was in diabetischen Betazellen schiefläuft und setzen damit neue Maßstäbe, wie Studien auf diesem Gebiet in Zukunft durchgeführt werden sollten.“ Und weiter sagt Prof. Michele Solimena, einer der vier führenden Forscher dieser Studie: „Wir sind zuversichtlich, dass unser Ansatz letztendlich eine neue Sichtweise dafür liefern wird, wie die Exposition von Betazellen gegenüber Nahrstoffüberlastung deren Funktion über längere Zeit verschleißen wird und damit ihre Fähigkeit beeinträchtigt, den übermäßigen Bedarf an Insulin zur Aufrechterhaltung der metabolischen Homöostase zu decken.“ Das Ziel des IMIDIA-Konsortiums, das von Februar 2010 bis September 2016 insgesamt 14 europäische akademische Institutionen, große Pharmaunternehmen und Biotech- Unternehmen umfasste, war die Identifizierung neuer Wege zur Regeneration, Erhaltung und zum Schutz von insulinproduzierenden pankreatischen Betazellen als Mittel zur Beschleunigung der Entdeckung von effektiveren Strategien zur Prävention und Behandlung von Typ-2-Diabetes. Eine Hauptaufgabe des IMIDIA-Konsortiums bestand darin, zu definieren, welche Gene in Betazellen von diabetischen Patienten im Vergleich zu Betazellen von nicht-diabetischen Patienten abnormal exprimiert werden. Die veränderte Expression dieser Gene konnte dann für das Betazellversagen bei Diabetes verantwortlich sein. Erstmals basierten die Forscher ihre vergleichende Genexpressionsanalyse nicht nur auf Inselzellen, die von nicht-diabetischen und diabetischen Organspendern gesammelt wurden und für die die Verfügbarkeit klinischer Informationen begrenzt ist, sondern sie basierten auch auf Inselzellen von Patienten, die sich einer Bauchspeicheldrüsenoperation unterziehen mussten. Für die letztgenannten Patienten lagen eingehende medizinische Informationen vor, und der Diabetes-Status konnte ebenfalls unmittelbar vor der Operation genau beurteilt werden. Dieser Ansatz ermöglichte es daher, die größte Sammlung von Inselzellen aus nichtdiabetischen und diabetischen, aber auch aus prädiabetischen Personen zu erstellen. Mit Hilfe dieser Proben identifizierten die Forscher 19 Gene, deren Expression sowohl in den Inselzellen der diabetischen Organspender als auch in denen der diabetischen chirurgischen Patienten im Vergleich zu denen nicht-diabetischer Spender und Patienten verändert wurde. Neun dieser 19 Gene waren bisher noch nie in diabetischen Inselzellen als dysreguliert beschrieben. Allerdings konnte die Studie keinen Beweis dafür finden, dass eines dieser Gene in Inselzellen von prädiabetischen Probanden dysreguliert vorliegt. Das könnte darauf hindeuten, dass ihre geänderte Expression eher eine Konsequenz als die Ursache des Betazellausfalls im Diabetes ist. Zukünftige Studien sollen daher untersuchen, welche Gene vor dem Absterben der Betazellen fehlreguliert sind. Dazu müssen aber mehr Inselzellen von prädiabetischen Probanden gesammelt werden, und genau das ist eine der Hauptaufgaben des kürzlich ins Leben gerufenen EU-IMI-Konsortiums RHAPSODY, dem alle vier Teams angehören, die als Partner die vorliegende IMIDIA-Studie leiten.
Über IMIDIA:
IMIDIA ("Innovative Medicines Initiative for Diabetes", www.imidia.org) ist ein öffentlich-privates Konsortium, das von der Initiative Innovative Medicines Initiative (IMI) finanziert und von Sanofi, Servier und der Universität Lausanne geleitet wird. Führende europäische Betazell-Experten aus 14 akademischen Institutionen, acht Pharma-Forschungseinrichtungen sowie eines Biotechunternehmens haben sich dabei offiziell im Rahmen des IMIDIA-Projekts zur Diabetesbekämpfung zusammengeschlossen. IMIDIA arbeitet an der Entwicklung neuartiger, patientenorientierter Werkzeuge, Biomarkern und grundlegendem Wissen über die Organisation von Betazellen, um den Weg zu einem verbesserten Diabetesmanagement zu ebnen. Es handelt sich um eine einzigartige Zusammenarbeit führender europäischer Forschungsgruppen, die sich auf die notwendigen Innovationen konzentriert, diese eng an die Anwendung koppelt und evaluiert, um dadurch neue Diagnostika, Prognosen und Therapeutika zu entwickeln. Rund 100 Forscher beschäftigen sich in sechs verschiedenen wissenschaftlichen Arbeitspaketen mit neuartigen Ansätzen, wie z.B. bildgebenden Biomarkern, Systembiologie und Signalweganalysen. Alle mit dem Ziel, patientenrelevante in vitro und in vivo Krankheitsmodelle sowie Biomarker zur Überwachung des Krankheitsverlaufs und der Therapie zu entwickeln. IMIDIA-Teilnehmer waren AstraZeneca, Boehringer Ingelheim, die französische Atomenergiebehörde (CEA), die Medizinische Hochschule Hannover, das Imperial College London, Lilly, das Nationale Zentrum für wissenschaftliche Forschung (CNRS), das Nationale Institut für Gesundheit und medizinische Forschung (INSERM) , Novo Nordisk, Roche, Sanofi, Sarl Endocells, Servier, SIB-Schweizer Institut für Bioinformatik, Vrije Universität Brüssel, Technische Universität Dresden, Universität Genf, Universität Lausanne, Universität Paris Diderot und Universität Pisa. Zusätzliche finanzielle Unterstützung für diese Studie kam durch das Deutsche Zentrum für Diabetesforschung (DZD eV), das vom Bundesministerium für Bildung und Forschung unterstutzt wird, dem italienischen Ministerium für Bildung und Forschung sowie vom Wellcome Trust, dem Medical Research Council und der Royal Society in Großbritannien.
Publikation
Titel: “Systems biology of the IMIDIA biobank from organ donors and pancreatectomised patients defines a novel transcriptomic signature of islets from individuals with type 2 diabetes”
Solimena et al.2017, Diabetologia, DOI: https://doi.org/10.1007/s00125-017-4500-3
Hidden link for journalists:
http://www.diabetologia-journal.org/files/solimena.pdf
Link article on SpringerLink
http://link.springer.com/article/10.1007/s00125-017-4500-3
Corresponding Authors
Prof. Dr. Michele Solimena
Paul Langerhans Institute Dresden of the Helmholtz Center Munich at University Hospital Carl Gustav Carus and Faculty of Medicine TU Dresden
Fetscherstrasse 74
01307 Dresden, Germany
Email:
Dr. Anke Schulte
Sanofi-Aventis Deutschland GmbH
Diabetes Research
Industriepark Höchst, Building H821,
65926 Frankfurt am Main, Germany
Email:
Dr. Mark Ibberson
Vital-IT Group, SIB Swiss Institute of Bioinformatics
Quartier Sorge, batiment Genopode,
1015 Lausanne, Switzerland
Email:
Prof. Dr. Piero Marchetti
Department of Clinical and Experimental Medicine
Cisanello University Hospital
University of Pisa
Via Paradisa 2
56126 Pisa, Italy
Email:
Pressekontakt
Dr. Frank Möller
Wissenschaftlicher Koordinator Paul Langerhans Institut Dresden
Tel.: +49 (0)351 796 5634
Email:
