Nov 11, 2023
Episode 11: Seeing and being seen - A debate on the latest research approaches to visual impairments
Our podcast series you ask we explain - Touching fears in medicine started in January and is published monthly. In the 11th episode, as part of the 14th Retina Day, we discussed the topic: Seeing and being seen - A debate on the latest research approaches to visual impairments .
We wanted to discuss with you and answer your questions. Didn't have time to be there? No problem: just listen to our podcast on the go - on Spotify, Apple Music, Deezer or here.
Stephan Wiegand : Ein Podcast der Medizinischen Fakultät der TU Dresden in Kooperation mit der Sächsischen Zeitung, dem COSMO Wissenschaftsforum und den Städtischen Bibliotheken Dresden.
Karen Teßmer: (...) Hallo und herzlich willkommen auch noch mal von meiner Seite. Mein Name ist Karen Teßmer und ich freue mich sehr, heute stellvertretend für alle, die Sie hier im Raum sitzen und für alle Hörer des Podcasts You Ask We explain mit unseren Experten zu reden. Ich sitze hier, wie Sie sehen, mit Rednerinnen des heutigen PRO-RETINA-Informationstags, mit Ruth Forschbach, mit dem Privatdozent Thomas Ach aus Bonn, dem Oberarzt Dirk Sandner und dem Professor Mike Karl. Ich selbst bin Postdoktorandin, also wissenschaftliche Mitarbeiterin hier am Zentrum für regenerative Therapien in Dresden. Und ich arbeite in der Arbeitsgruppe von Professor Marius Ader, den Sie schon hier zwischenzeitlich immer ebenfalls in der Moderation gesehen haben und gehört. Wir arbeiten bei uns in der Arbeitsgruppe, unter anderem auch in Kollaboration mit Professor Mike Karl, der ebenfalls eine Arbeitsgruppe in Dresden hat, am Deutschen Zentrum für Neurodegenerative Erkrankungen. Und deswegen hier direkt ein kleiner Disclaimer: Unser Arbeitsalltag findet ja größtenteils auf Englisch statt, in der Forschung und dementsprechend auch ohne Siezen. Also wundern Sie sich nicht, wenn ich Mike zwischenzeitlich Duze und die anderen Redner Sieze aus Höflichkeitsgründen. Das heißt nicht, dass ich zu dir unhöflich sein möchte. Genau. Leider müssen Mike und Herr Ach heute etwas vorzeitig abreisen. Deswegen würde ich ausnahmsweise nicht mit unserem weiblichen Gast beginnen, sondern uns direkt den Herren in der Runde zuwenden. Deswegen auch an das Publikum im Saal, wundern Sie sich also bitte nicht, wenn Mike und Herr Ach im Laufe der Veranstaltung klammheimlich still und leise ihre Plätze verlassen. Fangen wir doch vielleicht einfach mit Mike an. Mike ist das, was man bei uns tendenziell als einen Clinical Scientist bezeichnen würde oder hat zumindest so angefangen. Er hat in Hamburg Medizin studiert, eine medizinische Doktorarbeit verfasst und ist währenddessen und danach in der Forschung hängengeblieben. Nach einem längeren Forschungsaufenthalt in Seattle ist er dann 2010 nach Dresden gekommen und hat dort dann nach kurzer Zeit seine eigene Arbeitsgruppe aufgemacht und ist seit 2020 auch Professor an der TU Dresden und forscht daran, menschliche Mininetzhäute wachsen zu lassen. Und die werden zum einen genutzt, um retinale Degenerationserkrankungen zu modellieren und aber auch um therapeutische Ansätze wie Gen- oder Zelltherapie zu testen. Und Mike du bist ja schon jetzt ziemlich lange in der Forschung mit dabei. Was hat dich am Anfang dazu motiviert, damit überhaupt anzufangen? Und über diesen Zeitraum, Was würdest du sagen? Wie hat sich die Forschung in diesem Bereich verändert? Gibt es da große Entwicklungen, die dich besonders beeindruckt haben?
Mike O. Karl: Ja, vielen Dank erst mal für die Einladung und die spannende Frage. Da gibt es natürlich eine persönliche Perspektive zu. Und es gibt vielleicht auch in der Rückschau dann immer wieder eine professionelle aus meiner heutigen Sicht damals war die Motivation mit Sicherheit. In der Medizin war es halt so man hat angefangen zu studieren und hat in einer Vielzahl von Informationen durchflutet. Aber am Ende ist ja die Frage, wie kann ich dem Patienten am besten helfen? Und dann sind bei den Medizinstudierenden am Anfang die Motivation sehr unterschiedlich. Patienten helfen kann man natürlich, indem man in der Klinik mit dem Patienten zusammenarbeitet. Das andere ist aber, wir können auch versuchen, daran zu arbeiten, Therapien zu entwickeln, die nicht vorhanden sind. Und meine persönliche Motivation war der zweite Teil. Ich bin auch mehr oder weniger über die Biologie und Physik zur Medizin gekommen. Und ich glaube, das Medizinstudium ist am Anfang ein sehr breiter Fächer. Begeistert hat mich in der Karriere vermutlich am meisten die Möglichkeit, können wir Systeme entwickeln mit menschlichen Zellen? Und als ich damals angefangen habe, gab es das sogenannte Tissue-Engineering. Wir haben uns also Zellen gebastelt aus vorhandenen Geweben, die da sind. Und das ist eine Ära gewesen, die dann zu Ende gegangen ist, weil man einfach gemerkt hat, man kann jetzt nicht Zellen nehmen vom Patienten, so einfach oder aus Tieren und die lange in Zellkultur aufbewahren. Dann ist ein gewisser Teil davon übrig geblieben. Aber die stammzellbasierten Systeme, die waren schon sozusagen eine Revolution und die haben mit Sicherheit meine Karriere dann bestimmt. Das fing eigentlich alles an mit einem Interesse für Entwicklungsbiologie. Wie entwickelt sich eigentlich so ein Auge? Das Grundinteresse war, da mitzumachen, wo schon seit langer Tradition Wissenschaft stattgefunden hat. Denn die Entwicklungsbiologie, die gibt es halt schon sehr, sehr lange seit Beginn. Aber die Frage dann zu sagen, man geht eher in die Richtung Engineering und können wir Gewebe herstellen, die hat sich erst dann mit den neuen Technologien ergeben. Das würde ich sagen, ist so der die zwei Facetten für die Frage.
Karen Teßmer: Okay spannend. Herr Ach, Sie sind ja auch ausgebildeter Mediziner. In Ihrer Doktorarbeit habe ich gesehen, haben Sie sich aber noch mit Brustkrebs beschäftigt und wurden dann aber trotzdem relativ schnell beim Europäischen Ophthalmology Board Fellow und haben auch im Themenbereich der Retina dann habilitiert. Und parallel zu Ihrer Arbeit haben Sie ja verschiedenste Weiterbildungen gemacht im Bereich der klinischen Studien, Management klinischer Studien, Medikamentenentwicklung und auch als Spezialist für Bestrahlungen, auch besonders im Kontext von den Augen. Sie wissen also sehr, sehr gut Bescheid darüber, was aktuell und in Zukunft in der Behandlung von Erkrankungen möglich ist und sein wird. Die andere Seite sozusagen von dem, was Mike dann im Endeffekt gemacht hat, aber trotzdem ein ähnliches Thema. Sie haben es zwar im Talk schon so ein bisschen erzählt, aber vielleicht für das Audiopublikum auch noch mal: Kann AMD Stand jetzt eigentlich geheilt werden? Und hat die Arbeit in diesem Kontext eigentlich ihre eigene Wahrnehmung der Sinne verändert?
Thomas Ach: Jetzt weiß ich nicht, ob ich das mit dem Brustkrebs wieder beginnen soll. Also man beginnt ja das Studium sehr breit gefächert und durchläuft mehrere Praktika. Eigentlich ja alle Praktika in einem Humanmedizin-Studiengang und ich dachte eigentlich, dass die Gynäkologie genau das ist, was ich brauche. Allerdings war das Praktikum so schlecht, dass ich mich überhaupt nicht in der Gynäkologie wiedergefunden habe, aber die Doktorarbeit tatsächlich hier beendet hatte. Das war bereits in der Doktorarbeit eine experimentelle Arbeit. Wir haben uns sehr viel mit Zellen beschäftigt, versucht also bösartige Brustkrebszellen ist immer besser zu machen, mit entsprechenden Umwandlungen. Zellen zu verändern, damit sie nicht mehr so aggressiv sind und ihre bösartigen Veränderungen nicht weiter fortsetzen können. Das hat mich immer begeistert. Auch die Wissenschaft heraus und war eigentlich überhaupt nicht dafür, Wissenschaftler zu werden, sondern wollte Kliniker werden und Patienten behandeln. Und dann gab es ein unheimlich tolles Augenpraktikum und das hat mich eigentlich vom ersten Moment an total begeistert, weil sie mit wahnsinnig innovativen Techniken in der Augenheilkunde. Denken Sie noch einmal an die OCT Untersuchungen, die ich Ihnen heute gezeigt hatte, mit einer wahnsinnigen Präzision ihre Netzhaut darstellen können. Und von dem Moment noch nicht ganz, wusste ich, dass ich Augenarzt werden wollte, sondern ich habe tatsächlich im Praktikum eine Augen-OP gesehen, wie das abläuft und mit welcher Mikrochirurgie sie am Auge operieren können. Und da wusste ich… Ich habe meine Eltern angerufen und wusste an diesem Abend Ich werde Augenarzt. Und das hat mich nicht mehr losgelassen. Wir haben das Glück und da, glaube ich, spreche ich mit Herrn Sandner aus einem Munde. Wir haben ja sogar zwei Organe. Wir müssen uns nicht nur auf ein Herz beschränken, sondern haben zwei Augen. Und wenn man das mal unter der Spaltlampe sieht, das, was der Augenarzt da mit ihnen macht, dann finde ich das so unheimlich ästhetisch, ein riesengroßes Auge zu sehen mit den Veränderungen. Und wir leben tatsächlich von Blickdiagnosen. Wir gucken auf das Auge und wir müssen Diagnosen treffen innerhalb weniger Sekunden. Und das gelingt ja auch meistens mit viel Übung eigentlich ganz gut. Zur Therapie, da ging es jetzt in Richtung Makuladegeneration. Das ist ja, was uns beschäftigt. Wir haben, wir werden alle älter, wir erwarten Millionen von Betroffenen. Wir haben bereits jetzt 5 bis 7 Millionen Betroffene in Deutschland. Und wir werden älter und werden in den nächsten 20, 30 Jahren noch mehr Betroffene aufweisen. Und die Erblindung, die bei einer Nichtbehandlung ansteht, ist ja nicht das, was man anstreben sollte. Das hat ja wahnsinnige Auswirkungen auf unser Gesamtes, nicht nur Gesundheitswesen, sondern die gesamte Gesellschaft. Wir hatten in den letzten 15 Jahren unheimlich viel erreicht. Es ging los mit der Behandlung der feuchten Makuladegeneration. Da ist gerade meine Karriere losgegangen. Wir sind jetzt vielleicht mittendrin in meiner Karriere. Wir werden jetzt anfangen, die trockene Form der Makuladegeneration tatsächlich zum Ersten Mal vielleicht zu verlangsamen. Nicht ganz zum Stillstand zu bekommen. Und die letzten 22 Jahre meiner Karriere, denke ich also bin ich wahnsinnig überzeugt davon, dass wir in 20 Jahren Präparate zur Verfügung haben, die uns helfen werden, diese negativen Veränderungen bereits sehr frühzeitig zumindest positiv zu beeinflussen. Dass diese schweren Verläufe mit der Vernarbung zum Schluss, egal ob in der feuchten oder in der trockenen Form einfach nicht auftreten werden oder sehr spät auftreten werden, dass man auch lange am gesellschaftlichen Leben teilhaben kann.
Karen Teßmer: (...) Ja, danke für die Meinung dazu. Wenn man das so hört, dann frage ich mich immer Sie kommen beide aus, quasi aus dem gleichen originalen Punkt, aber sind dann aufgefächert. Der eine ist in der Klinik geblieben, der andere ist in die Forschung gegangen. Aber am Ende des Tages arbeiten sie beide sehr stark noch im Kontext AMD an dem gleichen Thema. Wie ist das denn eigentlich mit der Klinik und der Forschung an sich? Wie stark ist da die Interaktion? Wie schnell kommen Informationen aus der Forschung in die Klinik und aus der Klinik zurück in die Forschung?
Thomas Ach: Ja, in so einer großen Klinik wie Bonn sicherlich sehr schnell. Es ist ja ein sehr wissenschaftsstarker Standort, auch die Klinik dementsprechend ausgerichtet, sodass Ideen, die in der Basiswissenschaft in der Grundlagenwissenschaft entstehen, auch sehr schnell über Projekte Förderprojekte in die Realität umgesetzt werden können. Man muss aber verstehen, das haben Sie hoffentlich heute auch mitbekommen, dass solche Projekte, dass die Ideen dazu die Entwicklungen dazu, Zeit in Anspruch nehmen. Sie brauchen nicht nur die Idee, sie brauchen auch das Geld dazu. Das muss ihn irgendjemand geben. Sie brauchen Personal, das das mitarbeitet. Und plötzlich sind aus Ideen Jahre, die ins Land ziehen, aus denen hoffentlich dann weitere Ideen, Produkte entstehen, Patente entstehen, aus denen sie Firmen gründen können oder das auch in die Kommerzialisierung weiter vorantreiben können. Und ich hatte ja heute auch schon mal diese Patente angesprochen. 20 Jahre. Wenn Sie heute denken, das ist zwar ein langer Zeitraum, aber bis Sie da anfangen von der Idee, die Sie patentieren, da haben Sie gerade 20 Jahre Zeit, damit auch vielleicht ein bisschen Geld zu machen. Da geht die Zeit relativ rasch ins Land, gerade bei Erkrankungen, die auch sich nicht von heute auf morgen verändern. Diese Verbindung zwischen der Grundlagenwissenschaft und der Klinik ist ein unheimlich wichtiger Punkt, der sicherlich in Deutschland zentral an den Universitäten stattfinden wird, auch in Zukunft stattfinden wird. Und diese Strukturen gilt es zu unterstützen, Auch so attraktiv zu machen, dass Leute in diesen Strukturen auch bleiben möchten und nicht rausgehen und kein Interesse mehr an der Wissenschaft haben. Denn ohne die Wissenschaft und ohne die Weiterentwicklung wird es nichts geben. Man wird Ihnen alles verkaufen können, solange es nicht vernünftige Präparate oder Therapien gibt für verschiedene Erkrankungen.
Karen Teßmer: Ja, das stimmt auf jeden Fall. Da sprechen Sie auch einen weiteren Punkt an, das so ein bisschen dieses nomadische Verhalten, was auch manchmal gebraucht wird, aber was natürlich positive und negative Aspekte mit sich bringen kann, von Leuten, die in der Forschung arbeiten und ich denke mal auch ein Stück weit bei den Klinikern ist das vielleicht auch der Fall. Sie haben ja auch häufig mehrere Stationen, die sie durchlaufen, und verschiedene Orte, die sie sehen. Wie ist das denn zum Beispiel bei dir jetzt gewesen? Also würdest du sagen retrospektiv, diese Bewegung, die du in deiner Karriere hattest, wie stark sind die positiv oder negativ zu werten? Und gibt es da Sachen, die du vielleicht auch aus deinem Aufenthalt in Seattle mitgenommen hast oder mitnehmen würdest, die man vielleicht hier noch etablieren sollte. Oder Impulse, die irgendwie hilfreich wären.
Mike O. Karl: Zu dem Thema könnte ich jetzt lossprudeln. Eine fokussierte Antwort ist da zum Teil gar nicht so einfach. Aber erstmal zu meiner Karriere. Ich würde sagen, ich saß immer auf der Mauer. Auf der rechten Seite konnte ich in die Klinik fallen und die linke Seite in die Grundlagenforschung. Und das sage ich jetzt ein bisschen übertrieben, weil die Mauer halt sehr schmal war. Und wir müssen dafür sorgen, dass das breiter wird in der Mitte, damit das nicht so passiert. Und diese Mitte zu stabilisieren war eine lange Zeit lang ein großes Thema. Immer. Weil so wie ich jetzt gerade gesagt hat, das Geschwindigkeit ist ja alles und Zeit ist auch das nächste. Aber wir sind mittlerweile sehr, sehr komplex geworden. Und um ein Beispiel zu machen jetzt es geht nicht nur um Klinik und Grundlage, sondern es geht sogar mittlerweile interdisziplinär. Also zwischen den unterschiedlichen Fachbereichen reden wir jetzt über ganz andere Dinge noch. Ich wollte das in meinem Vortrag auch vorstellen, aber habe ich gedacht, es wird dann zu viel, dass alles so schnell runterzubrechen. Aber mit der Frage kann ich das kurz mal ansprechen. Also wenn wir zum Beispiel ein Konsortium entwickeln, in dem wir beide auch gemeinsam zusammen interagieren, wo es aber darum geht, sogar noch größer zu denken, weil am Ende sind die Expertisen, die gebraucht werden, unglaublich vielfältig. Das heißt, ich betrachte das mittlerweile. Wir müssen besser darin werden, Megaprojekte zu haben und Megaprojekte. Klingt jetzt erstmal so riesig nach dem Motto Ja, wir wollen jetzt sonst irgendwas machen. Aber der Punkt ist, Wenn ich einen Physiker brauche und Bioinformatiker brauche und Chemiker brauche. Und so weiter und so fort, dann kann ich nicht versuchen, mir immer diese Expertise anzueignen und zu glauben, ich kann das alles alleine lösen. Das war in der Vergangenheit öfter mal der Fall, aber mittlerweile sind die Themenfelder viel, viel größer und wir müssen da mehr interagieren. Und da sind auch noch neue Formen, wie wir das tun können, jetzt in Entwicklung. Ich würde unser Konsortium, was wir zum Beispiel haben, eher als Testfeld bezeichnen. Wir sind am Anfang zu lernen, Wie können wir da noch viel besser werden? In der Wissenschaft sagt man immer, man versackt zum Teil in Silos. Die einen kümmern sich um das, was sie am besten können. Aber das Spannende ist ja eigentlich Wissenschaft bewegt sich da am schnellsten vorwärts, wo man miteinander in Interaktion kommt und die Verbindung zwischen Grundlage und Klinik. Früher war es so, wenn wir nur Tiermodelle haben, einen Kliniker dazu zu motivieren, das ist einerseits natürlich auch nicht nur eine Frage von Motivation, aber auch von Expertise. Jetzt mit den humanen Modellen schließt sich da vielleicht eine Lücke, aber wir müssen auch gucken, ob das alles passiert. Und wenn es dann darum geht, neben dem Wissenserkennen. Also wir können jetzt herausfinden, wie das auch so ist, braucht man am Ende auch eine Industrie, die das umsetzt. Und die sitzt sozusagen jetzt nicht an einem Universitätsklinikum. Entweder muss das dann aus uns selbst rauskommen, da sind noch viele Punkte, wo Zeit eingespart werden könnte. Wo wir gerade drüber gesprochen haben, das war das, was Herr Ach sagte und da sind wir jetzt glaube ich gut dabei. Aber da sind halt auch in den unterschiedlichen Feldern, was interdisziplinär heißt, unterschiedliche Bedürfnisse. Die Kulturen der Wissenschaft sind sehr unterschiedlich Und das kostet alles Zeit auch zu lernen, miteinander zu reden. Denn wenn ich mit einem Bioinformatiker rede, der wird mir von Dingen erzählen, habe ich keine Ahnung von und umgekehrt auch nicht. Und dieses linke Auge, blind, rechte Auge, blind, wie wir das bezeichnen, das braucht Zeit und Räume, wo wir miteinander interagieren können. Und die müssen dann geschaffen werden, dass das auch längerfristig dann substanziell ist, nachhaltig.
Karen Teßmer: Wenn all diese Menschen erwähnt werden, die da eine Rolle spielen. Wie wichtig ist denn in deinem Fall und wie wichtig ist bei Ihrem Fall Herr Ach dann die Interaktion mit den Patienten in dem Kontext der Forschung eigentlich.
Thomas Ach: Nicht der Kontext, sondern das Gespräch mit dem Patienten ist in so einer großen Universitätsklinik immer extrem wichtig, weil wir sie als Betroffene natürlich auch brauchen, um Studien auch durchzuführen. Also sind das ja meistens Studien, die bereits in den klinischen Phasen sind. Solche Zulassungen durchlaufen mehrere, mehrere Phasen, bis letztendlich Präparate auch eine Zulassung erfahren. Und dafür sind immer wieder auch Freiwillige gesucht. Und die bekommen sie ja nur, indem sie im Gespräch mit dem Patienten das auch anbieten. Entsprechende Strukturen auch vorhalten, Studienambulanzen vorhalten, die ihnen das ermöglichen, dass Patienten hier auch tatsächlich Zugang zu Medikamenten bekommen, die es eben noch nicht auf dem Markt gibt. Also ohne Patient wird es keine Studien geben. Ohne Studien gibt es keinen Patienten.
Karen Teßmer: In diesem Sinne vielleicht auch vielen Dank noch mal an Sie alle, dass Sie heute hergekommen sind, um sich über diese ganzen Dinge zu informieren und um das Interesse zu zeigen. Es geht dann ja auch immer in beide Richtungen, die Interaktion. Also schön, dass Sie alle da sind.
Thomas Ach: Vielleicht kommt auch noch mal eine Lanze für die Studienambulanzen und auch die Studientätigkeiten treffen. Sie werden vermutlich in keiner anderen Begebenheit besser betreut als tatsächlich einer Studie. Sie werden so viele Besuche an den Kliniken durchlaufen, weil sie auch kostenlos oder vielleicht sogar mit ein bisschen Zugewinn für sie, also finanzielle Entschädigung. Aber sie werden so genau kontrolliert, haben Zugang zu den neuesten Produkten, die es hoffentlich auch auf dem Markt geben wird und die sich positiv in den Studien zeigen. Also ich kann nur werben dafür, auch wenn es Möglichkeiten gibt und sie da angesprochen werden, sich das tatsächlich auch anzuhören.
Karen Teßmer: Ja, Herr Sandner, Sie sind ja ebenfalls ausgebildeter Mediziner und sind ja seit Ihrem Medizinstudium, wenn ich das richtig gelesen habe, eigentlich schon immer komplett auf die Augen fixiert. Direkt im Anschluss an das Medizinstudium hat Herr Sandner nämlich seine Facharztausbildung in der Ophthalmologie in Leipzig begonnen und ist seit 2005 Oberarzt in Dresden und dort operativ spezialisiert auf die Vitrio-Retinale-Chirurgie. Genau. Also ich denke, in dieser Runde sind Sie also derjenige, der an den Patienten wirklich am allernächsten dran ist. Vielleicht deswegen an Sie. Die Frage Was deutet eigentlich so ganz banal gefragt auf eine Augenerkrankung hin? Ab wann sollte ich zum Arzt gehen? Und was freut Sie in der Interaktion mit Ihren Patienten eigentlich am meisten?
Dirk Sandner: Das ist, wenn ich erlebe Das, was wir gemacht haben, hat eine gewisse Verbesserung für den Patienten. Der Patient spiegelt mehr die Behandlung, die ich gemacht hab, auch wenn ich es vielleicht nur aufgehalten habe oder verlangsamt habe. Oder es ist wieder ein Stück besser geworden. Ich kann dort quasi mit dem, was ich täglich mache, ein Stückchen Sehleistung zurückgewinnen, erhalten, den kompletten Verlust vermeiden. Und das sind so die schönsten Momente, wo man jetzt dann auch, auch wenn der Tag zwölf Stunden hat, quasi immer abgespannt nach Hause kommt, wo man dann aber mit einer gewissen Befriedigung nach Hause kommt und sagt okay, das lohnt sich der Aufwand und letztlich das, was ich ja schwierig ist, dass es eben trotz aller Bemühungen Patienten gibt, wo wir noch nicht so weit sind, die wir nicht glücklich machen können. Wo wir eben auch sagen können, wir haben zurzeit nichts oder wir haben alles ausgereizt und es geht eben doch in eine gewisse Richtung weiter und es wird schlechter und der Patient merkt das auch und Wir haben aber noch nichts, was wir ihm anbieten können. Und da ist natürlich dann der Kreis hier zur Grundlagenforschung, dass wir quasi dort durch die Interaktion dann zumindest Gedanken haben, Ideen haben, wie wir eben auch dieser Gruppe von Patienten dann eben perspektivisch vielleicht auch helfen können. Und letztlich, das macht es eben auch quasi die Zusammenarbeit jetzt mit dem CRTD, mit Mike, mit Marius. Letztlich macht das spannend dort. Ein kleiner Teil zu sein, auch wenn wir gesagt die Kollegen die Grundlagen schaffen und ich in dem Kontext quasi der bin, der quasi so ein bisschen operativ das umsetzt und eben guckt jetzt und unterm Strich, welche Ergebnisse oder welche Resultate können wir jetzt erst mal quasi im Modell jetzt erreichen. Und zu der ersten Frage Wann sollte ich zum Augenarzt? Ich sollte immer zum Arzt, wenn ich das Gefühl habe, hier stimmt irgendwas nicht. Gestern war es noch gut oder egal welche Veränderungen das ist und ich sollte sicher jetzt generell gesprochen, wenn ich keine Probleme habe, gut sehen kann. Also spätestens mit Mitte 40 irgendwann mal einen Augenarzt kontaktiert haben. Augendruck, Glaukom ist schleichend, muss ich nicht bemerken. Wenn in der Familie vielleicht irgendwelche Erkrankungen aufgetaucht sind, dann muss ich gehen. Ja.
Karen Teßmer: (...) Ich finde es sehr schön, dass wir trotz Bezug auf Augen und auf Sicht und Blicke diesen schönen anderen Sinneseindruck hier dabei haben und auch was für die Ohren geboten bekommen. Vielleicht in Bezug auf Sinneseindrücke. Mal zu Ihnen, Frau Forschbach. Sie sind studierte Kommunikationspsychologin, Autorin, Lyrikerin und seit über 20 Jahren aktives Mitglied bei dem Verein PRO-RETINA Deutschland, einer Selbsthilfevereinigung von Menschen mit Netzhautdegeneration. Und Sie leiten im Team die Landesgruppe Nordrhein Westfalen mit.
Ruth Forschbach: Nicht mehr.
Karen Teßmer: Nicht mehr. Na gut. Aber Sie haben.
Ruth Forschbach: Ja, das habe ich.
Karen Teßmer: Wie Sie ja auch in Ihrem Vortrag erzählt haben, sind Sie selbst Betroffene der Myopie, also der Kurzsichtigkeit. Und da stellt sich für Leute, die davon nicht betroffen sind, wie sicherlich bei unseren Zuhörern auch viele dabei sein werden, auch immer die Frage, wenn man von so einer Erkrankung betroffen ist. Wie gut gelingt es Ihnen denn eigentlich, Ihren Sehverlust auszugleichen und auf welchem Weg tun Sie das im Normalfall?
Ruth Forschbach: Ich sage Ich hatte Glück im Unglück. Ich habe natürlich auch auf dem linken Auge eine Makuladegeneration aufgrund der hohen Kurzsichtigkeit. Das ist gar nicht wegzudenken. Es gelingt mir mehr als auszugleichen, gelingt mir mal mehr und mal weniger gut, weil das rechte Auge ist das Auge, was mein Führ-Auge ist. Das heißt mit anderen Worten, es mischt sich immer mal wieder in den Vordergrund, weil es sagt Du darfst mich nicht vernachlässigen. Jetzt bin ich dran. Und wenn ich dann diesen miesen Seheindruck habe, dann ist es schwierig für mich. Was ich aber glaube, womit ich das bewältigen kann, ist, dass ich eine sehr starke Resilienz habe. Ich hatte es ja versucht, in meinem kleinen Vortrag ein bisschen zu beschreiben. Wenn so ein massiver und damals für mich wirklich unvorhergesehener Sehverlust mich ereilt hat und wie die anderen Menschen es auch erlitten haben, dann braucht es erst mal so ein Wiederkäuen. So würde ich das benennen. Also erst mal durch dieses Tal gehen, Ja, und dann aber sagen Was mache ich jetzt? Ich bin Ihnen für Ihre Vorlage sehr dankbar. Lieber Herr Sandner, Sie sagen, ich bin glücklich, wenn ich Menschen glücklich machen kann, Patienten glücklich machen kann. Das kann mir nicht immer gelingen. Aber was glücklich machen kann, ist einfach. Auch wenn Sie jetzt nichts anbieten können. Auch Sie, Herr Professor Ach, oder Sie Herr Professor Karl, das sind alles wunderbare Ansätze. Aber wir müssen jetzt leben. Und das, was Sie machen, ist unglaublich großartig. Also, es gibt ganz viel Hoffnung. Das weckt etwas. Aber ich muss jetzt leben. Ich kann nicht warten. Bis in zehn Jahren weiß ich, was kommt. Das ist toll. Aber ich muss es jetzt leben. Und da hat mir. Und jetzt muss ich mal wieder eine Lanze für die PRO-RETINA brechen wirklich PRO-RETINA geholfen. Das heißt, was kann ich jetzt tun, um mein Leben noch so zu gestalten und lebenswert zu machen? Denn da gibt es ganz viel, denn ich bin ja nicht nur Auge, wie Sie eben gehört haben. Es gibt ja noch ganz viel von mir.
Karen Teßmer: Das heißt auch, wenn man zum Beispiel Informationen sucht zu wie kann man eigentlich mit Erkrankungen wie der Kurzsichtigkeit zum Beispiel Ausbildung in bestimmten Berufsbereichen machen oder sowas? Dann ist die PRO-RWTINA da auch eine gute Adresse.
Ruth Forschbach: Genau. Wir stehen ja, sag ich mal, auf ganz, ganz vielen Beinen. Also sozusagen wie so eine riesen Tausendfüßler. Wir haben ja für fast jede Netzhauterkrankung bestimmten Arbeitskreis. Und was das Wunderbare ja ist wir agieren ja als PRO-RETINA mit den wunderbaren Ärzten, Forscher, Wissenschaftlern zusammen. Und ja, das hilft uns und das hilft natürlich dann wieder hinaus den Betroffenen.
Karen Teßmer: Okay, also wer das hier hört und Interaktion sucht, ist bei der PRO-RETINA gut aufgehoben. Ich habe noch eine weitere Frage, weil Sie das vorhin erwähnt hatten, dass die Diagnostik, die Sie machen, natürlich extrem stark bildbasiert ist, was ja irgendwie eine gewisse Ironie ist in dem Kontext Wie sieht das denn eigentlich aus mit zukünftigen Entwicklungen? Also ist das was, wo Sie sagen das glauben Sie, dass das jetzt noch eine Weile so bleiben wird. Oder gibt es da auch Entwicklungen und Ansätze, solche Dinge zu automatisieren? Und glauben Sie, dass es hilfreich sein wird oder dass ein Stück weit Patienten dann auch selber schon, ich sag mal Heimdiagnostik ein Stück weit machen können?
Thomas Ach: Das ist ein ganz wichtiger Punkt, den Sie ansprechen. Also ich denke, ich werde auch in 22 Jahren noch Augenarzt sein und man wird mich vielleicht auch noch brauchen. Das werden die technischen Errungenschaften, die es geben wird, auch in 20 Jahren sicherlich nicht ablösen. Man kann aber heute mit der Bildgebung, die wir machen, jedes OCT, das wir von ihnen anfertigen, jede Aufnahme des Augenhintergrundes, die von ihnen angefertigt wird, das kann man natürlich über die künstliche Intelligenz, das ist ja in aller Munde, bearbeiten lassen, diagnostizieren lassen. Das ist jetzt für Deutschland vielleicht nicht das große Problem. Da haben wir eine kluge und gut ausgestattete, auch Dichte von Augenärzten. Aber wenn Sie an andere Länder denken, die also deutlich unterentwickelter sind als Deutschland, spielt das eine sehr große Rolle. Also man kann heutzutage mit einzelnen Aufnahmen des Augenhintergrundes bereits künstliche Intelligenz darüber laufen lassen, Computerprogramme darüber laufen lassen, die Ihnen sehr genau sagen können, welche Erkrankung oder welche Schwere der Erkrankung bei ihnen vorliegt und ob sie zeitnah auch einen Augenarzt aufsuchen sollten oder nicht. Also das läuft ja bereits. Da gibt es große Unterstützungsprogramme für Länder wie Afrika. Für Indien wird unheimlich viel dafür getan. Wir lernen natürlich auch aus unseren Bildern, aus jedem OCT-Schnitt. Den können Sie natürlich nehmen und auswerten lassen, was automatisiert natürlich viel besser geht. Es geht immer darum, aus diesen, aus dieser Unmenge an Daten, die sie generieren, natürlich neue sogenannte Biomarker zu entwickeln, also spezielle Veränderungen in den Bildern, die Sie vielleicht als Einzelner in einem Aufnahmeschnitt überhaupt nicht erkennen können, aber der Computer über viele Tausende und hunderttausende Aufnahmen generiert. Und aus denen können Sie tatsächlich wieder lernen, neue, nicht nur Diagnostik, sondern vielleicht auch therapeutische Ansätze zu entwickeln. Also die Forschung geht weiter. Man lernt immer wieder dazu. Jedes Bild, das man von ihnen aufnimmt, trägt dazu bei, dass die Forschung und die Entwicklung weitergeht. Zu dem sogenannten Home Monitoring, also können Sie auch zu Hause das aufnehmen, auch das gibt es bereits in den USA, also sogenannte OCT Geräte, die Ihnen quasi vom Versicherer von der Kasse zur Verfügung gestellt werden. Dass Sie zu Hause sich dieses Gerät dreimal die Woche ans Gesicht halten und ihr Augenhintergrund aufgenommen wird. Die Bilder werden automatisch an Auslesezentren gesendet und hier wird eine Entscheidung getroffen oder ein Alarm ausgelöst, wenn es in Richtung eines Wiederauftretens von Feuchtigkeit von Flüssigkeit geht. Da sind wir hier noch ein bisschen davon entfernt, aber die ersten Ansätze laufen und die laufen ziemlich gut.
Karen Teßmer: Okay, Frau Forschbach, Sie als Betroffene ist das was, dem Sie positiv oder etwas negativ entgegen?
Ruth Forschbach: Das ist doch spannend. Positiv, na klar.
Karen Teßmer: Sehr gut.
Ruth Forschbach: Ja.
Karen Teßmer: Und Sie, Herr Sandner?
Dirk Sandner: Ja, auf jeden Fall. Weil jetzt ist die Auswertung von der Datenmenge, die zur Verfügung steht. Es geht ja letztlich auch darum, welchen Patienten muss ich in welchen Intervallen quasi auch prognostizieren. Das ist einer, den muss ich engmaschiger führen, mit vielleicht dem und dem Medikament lieber als dem und dem. Und da muss ich erst dann und dann wieder gucken. Das sind spannende Fragen, wo wir jetzt noch keine Antworten haben. Aber ich sehe da schon, dass wir einfach über die Menge der Daten dann eben auch uns eher besser entscheiden können, individueller entscheiden können für den Patienten und damit letztlich die Ergebnisse noch besser werden, als wir es vielleicht jetzt schon können. Ja.
Thomas Ach: Ich hatte heute Morgen auch den Begriff der personalisierten Medizin, also zugeschnitten für Sie. Und da wird das sicherlich auch dazu beitragen können, dass man für Sie, für Ihre Erkrankung, für den Verlauf ihrer Erkrankung sehr zielgerichtet und zugeschneiderte Maßnahmen ergreifen wird.
Karen Teßmer: Ja, aus der ähnlichen Ecke vielleicht, wenn man jetzt nicht die Analyse sich anguckt, sondern die Behandlungsmethoden. Es kam ja glaube ich auch in einem Vortrag vor, eventuell mit solche Art von Chips, die man im Auge einpflanzen könnte? Das wird ja. Also das war eine Frage, die im Vornherein auch mal aufkam. Dieses Konzept von einem Cyborg, so mal extrem gesprochen. Wie ist das? Wo Sie sagen würden in der Klinik, denken Sie, dass das was ist, was in der Zukunft sehr relevant wird? Und ich weiß nicht, ob Sie Zeitaussichten geben können? Wahrscheinlich nicht.
Dirk Sandner: Aber es gibt letztlich jetzt. Es gibt für die für die atrophe Formen der Makuladegeneration letztlich aktuell Studien, die laufen wo eben einfach so ein Chip der quasi jetzt keine Elektroversorgung braucht, kein Kabel braucht, der unter die Netzhaut implantiert werden kann und eine Kamera nimmt das Bild auf, wandelt das in so ein Infrarotbild um und dieses Infrarotbild wird dann quasi auf diesen bionischen Chip projiziert und löst dort einen elektrischen Impuls aus. Und wenn die äußeren Netzhautschichten kaputt sind, dann kann normalerweise das Bild eben doch nicht entstehen. Aber die innere Netzhautschichten funktionieren noch, wo das Bild dann weitergeleitet wird. Und dieser Bereich, der kaputt ist, könnte vielleicht durch diesen Chip ersetzt werden. Und wenn das Signal dann quasi von den noch intakten Zellen aufgenommen wird, weitergeleitet wird, dann kann das zumindest einen gewissen Seheindruck in welcher Qualität auch immer generieren. Wie gut das sein wird, welche Komplikationen bei der.
Karen Teßmer: (...) Ich habe mich gefragt, wann das das erste Mal passiert. Da war mein Timer nicht ganz richtig.
Dirk Sandner: Wir warten auf die Ergebnisse letztlich und werden sehen, was eben auch in dieser Richtung möglich ist. Wie gesagt, Zellersatz ist natürlich noch mal spannender, einfach weil es dem, wie es die Natur vorgegeben hat, natürlich viel näher kommt. Vielleicht auch die Ergebnisse viel besser sein können. Aber das ist ein weiter Weg, der schon die letzten Jahrzehnte auch mit anderen Methoden untersucht wurde. Und auch da müssen wir gucken, dass wir weiterkommen. Ja.
Karen Teßmer: Danke schön. Da ist eine Wortmeldung auf der gegenüberliegenden Seite.
Stephan Wiegand : Ich habe Kärtchen eingesammelt bzw. meine Kollegin hat ein paar Kärtchen eingesammelt und es gibt tatsächlich Fragen aus dem Publikum und die würde ich gerne in die Runde mit einbringen. Eine davon ist Was halten Sie von einer minimalinvasiven Stimulation des vegetativen Nervensystems bei AMD (altersbedingte Makuladegeneration)?
Thomas Ach: Man kann nichts unversucht lassen. Machen Sie es. Wenn Sie das Gefühl haben, dass Ihnen das gut tut, dann tun Sie das. Wenn wir uns die Pathogenese der Makuladegeneration, also die Ursachen der Makuladegeneration, zugrunde legen, dann würde ich sagen, fehlt mir momentan so ein bisschen der Link dazu, warum das vegetative Nervensystem da auch die entscheidende Rolle mitspielen sollte. Die Veränderungen, die wir heute sehen und wahrnehmen, sind anderer Natur. Deshalb richtet sich das Hauptaugenmerk der Forschung auch auf diese Bereiche. Sie werden verschiedenste Möglichkeiten angeboten bekommen, auch in Zukunft über Lichttherapien, über Wohlfühloasen, die sicherlich am Auge auch für Wohlbefinden sorgen werden. Ob Sie damit allerdings Ihre Makuladegeneration und die negativen Veränderungen behandeln können, das würde ich, Stand heute etwas bezweifeln.
Stephan Wiegand : Zumindest trägt es zum Wohlfühlverhalten bei.
Thomas Ach: Ja, es kommt darauf an, wie viel Ihnen das wert ist. Ich meine, Sie können auch. Gehen Sie in ein Hotel und nutzen Sie den Spa Bereich und da massiert Sie auch jemand. Da fühlen Sie sich danach auch wohl. Und wenn Sie sagen, Sie möchten jemand anders das Geld geben, dann geben Sie es dem. Und…
Stephan Wiegand : Das war jetzt eindeutig Ja.
Thomas Ach: Na ja, solange nichts vorhanden ist. Also, wenn uns heute, ich sage noch mal, wenn wir heute Produkt A hätten, was Ihre Makuladegeneration stoppt und heilt, werden viele dieser anderen Therapien plötzlich komplett verschwinden, weil es keinen Absatz mehr dazu gibt. Aber wenn ich nichts habe, kann ich auch alles anbieten. Und sobald Sie sich besser fühlen und wohler fühlen und das ist ja erst mal komplett vorbei an der Schulmedizin, an jeglicher evidenzbasierten Medizin, da kann ich alles anbieten und ich werde immer jemanden finden, der sich bereitwillig auf meine Internetseite stellt und sagt Ich habe mich bei Herrn Ach total gut gefühlt und es was bringt oder nicht. Na ja.
Dirk Sandner: Das ist letztlich der Punkt, dass es quasi keine wirklichen Daten gibt, die jetzt Effektivität beweisen können. Und damit ist man irgendwo in dem Bereich, wo man auch glauben muss oder eben das probieren muss, die Möglichkeiten haben muss, das Ganze umzusetzen. Also ich, ich sehe das als Kliniker ein bisschen kritisch, aber ich würde das nicht sagen, wenn ich sage, ich möchte es machen und ich fühle mich wohl dabei, dann. Ja.
Thomas Ach: Also vielleicht noch mal um auch positiv in diese Richtung zu sprechen. Also Makuladegeneration. Es gibt die Veränderungen, die man sieht, diese Fettablagerungen, Das ist alles ziemlich nahe, auch an gefäßversorgenden Strukturen. Da kann man sich schon vorstellen, wenn sie jetzt anfangen, mit Therapie die Durchblutung zu verbessern, ob nicht doch auch Bereiche, die vorher vielleicht nicht ganz so gut durchblutet waren, vielleicht wieder etwas besser durchblutet sind. Aber eigentlich müssten Sie ja an den Ursachen ansetzen, die zur schlechten Durchblutung in der äußeren Netzhaut geführt haben. Da müssen Sie dran arbeiten. Das heißt, Sie werden mit vielleicht Verbesserung auch Ihres Nervensystems, vegetativen Nervensystems, durchblutungsfördernden Maßnahmen sicherlich kurzfristig Erfolg haben, aber die Zellen und das Gewebe, das bereits geschädigt ist. Das wird dadurch nicht wieder zur Jugendlichkeit zurückkehren, sondern sie werden kurzzeitige Verbesserung verspüren. Die Erkrankung wird vermutlich aber trotzdem weiter vorangehen.
Stephan Wiegand: Eine weitere Frage, die wir bekommen haben, ist: Die AMD Entzündungen sollen auch an der Entstehung eine Rolle spielen. Kann man das im Labor-Blut nachweisen? Geographische Atrophie? Wann ist es eine fortgeschrittene AMD?
Thomas Ach: Nun die fortgeschrittene AMD ist das Endstadium der AMD. Es sind letztendlich die geographische Atrophie, die trockene Makuladegeneration oder auf der anderen Seite die feuchte Makuladegeneration, exsudativ neovaskulär, auch in der Medizin genannt. Die Entzündungsreaktion, die spielt natürlich eine große Rolle. Also Kompliment ist ja eines der Hauptfaktoren. Sie können also bei Patienten mit Makuladegeneration ja auch erhöhte Komplementfaktoren in ihrem gesamten Kreislauf nachweisen. Es gab ja auch Versuche dazu mit entsprechender systemischer Therapie. Also stellen Sie sich vor, Sie nehmen nur noch Tabletten ein, die Ihr Komplementsystem unterdrücken. Das reicht aber nicht aus, um zumindest dann auch die Veränderungen am Auge signifikant zu beeinflussen. Sie brauchen das Medikament dann an einem Ort, an dem diese massiven Veränderungen auftreten. Und da ist die Spritztherapie in das Auge natürlich sehr willkommen. Also Entzündung spielt eine große Rolle, die Entzündungen aber auch wieder sicherlich eine Folge der grundlegenden Veränderungen im Gewebe verändert sich. Zellen verändert sich. Es werden Botenstoffe ausgeschickt, ausgesandt, die letztendlich zu entzündlichen Prozessen führen. Und ich würde es eher als eine Folge der Grunderkrankung sehen. Und gegen diese Folgen kämpfen momentan mit diesen Medikamenten und haben ganz gute Erfahrungen. Aber sie haben auch gelernt heute Wir können die Erkrankung nicht stoppen, wir können sie auch nicht zurückdrehen und das ist sicherlich ein Grund dafür. Wir müssen eigentlich an der Ursache weiter suchen und arbeiten.
Stephan Wiegand : Im linken Augenwinkel verfolge ich immer die Band, die schon wieder ein bisschen rumzickt. Aber ich hoffe, dass ich noch zwei Fragen durch kriege. Kann ein Katarak -Glaukom nach einem Hirninfarkt entstehen? Und was ist die beste Therapie?
Dirk Sandner: Also letztlich, dass Glaukom nach einem Hirninfarkt auftritt? Nein, aber der Hirninfarkt kann jetzt eine Sehverschlechterung hervorrufen, quasi mit Ausfällen, die denen ähnlich sind, wie sie beim Glaukom auftreten. Es gibt quasi Durchblutungsstörungen am Sehnerven, die letztlich auch Ausfälle machen können. Letztlich wo der Sehnerv sich dann auch verändert. Und die beste Therapie? Wie gesagt, ich hatte ja einige Punkte angesprochen. Wir müssen für jeden Patienten individuell entscheiden, in welchen… der Augendruck Ist der Hauptfaktor, den wir regulieren können. Auch wenn wie gesagt, bei manchen Patienten, die die Augendruckwerte scheinbar nicht das alleinige sind, warum das entsteht. Und wir müssen für jeden Patienten individuell entscheiden Wie hoch darf dieser Druck sein, damit der Schaden nicht weiter voranschreitet. Und da fängt man mit Tropfen an und wenn die Tropfen diesen scheinbar sicheren Bereich gut erreichen, dann ist die Tropfentherapie das, was am besten geeignet ist. Es gibt Laserbehandlungen, die man machen kann und wenn eben Tropfen, Laser nicht mehr ausreichend ist, man also noch über diesen Bereich ist, der scheinbar für den Patienten ausreicht, dann muss man zur Operation greifen. Und manchmal muss man diesen Bereich auch revidieren, dass man denkt okay, ich bin in dem Bereich und dann merke ich aber trotzdem, dass die Veränderungen voranschreiten, dass Ausfälle zunehmen und dann muss ich die neu definieren und muss dann meine Therapie an diese, an die neu definierten Bereich anpassen. Und auch da gibt es moderne neue Tropfen, die jetzt vor kurzem auf den Markt gekommen sind, die vielleicht noch ein bisschen mehr Wirksamkeit haben. Es gibt, wie gesagt, Laser und Operationen.
Stephan Wiegand : Gibt es einen Zusammenhang zwischen der Menière Krankheit und Krankheiten der Augen? Ist eine Menière Krankheit hinderlich bei der Heilung von Augenkrankheiten.
Dirk Sandner: Es gibt da schon gewisse Zusammenhänge. Das ist ja auch Form von Durchblutungsbeeinträchtigung. Und bei den Formen, wo gerade Glaukom bei niedrigen Augendruck entsteht, da spielen Durchblutungsveränderungen mit eine Rolle und dort gibt es eine gewisse Schnittmenge. Und wenn ich im Therapieansätze wähle, wo ich eben quasi generell die Durchblutungssituation mit Ginkgo Präparaten zum Beispiel verbessere. Auch das empfehlen wir manchmal. Kann ich letztlich dann zwei quasi Krankheitsbereiche vielleicht günstig beeinflussen?
Stephan Wiegand : Jetzt würde es passen, dass die Musik spielt, aber das tut sie nicht.
Karen Teßmer: (...) Ich bin immer noch ein bisschen fasziniert von den Einflüssen, die die Umwelt tatsächlich hat und die Interaktion mit der Umwelt für die Kurzsichtigkeit. Und dass es eben natürlich davon abhängt, ob man auch ab und zu mal in die Ferne schaut oder ob man viel immer nur auf die kurze Distanz schaut. Und von dem Draußen-Licht sozusagen. Wie ist denn das eigentlich? Ist das ausschließlich für die Kurzsichtigkeit ein Faktor oder gibt es auch andere Augenerkrankungen, wo das irgendwie eine besonders wichtige Rolle spielt?
Dirk Sandner: Kann man jetzt breiter fassen. Es gibt zum Beispiel Erkrankungen an der Hornhautoberfläche, also an dem Fenster, wo wir wissen jetzt, dass bei Patienten, die extrem viel draußen sind, quasi als Landarbeiter oder so, dass sich dort Veränderungen zeigen, die die normale Bindehaut auf die Hornhaut überwächst. Und da gibt es den direkten Zusammenhang mit Sonnenlicht Exposition also zu viel in dem Fall und dann eben einer gewissen Veränderung. Aber das ist reparabel, das kann man sozusagen abtragen und dann ist das mehr oder weniger repariert. Aber da gibt es eben auch zu viel Sonne, zu viel schädlich. Das andere ist, das Sonnenlicht hat natürlich auch einen hohen UV Anteil, letztlich Wellenlängen, wo quasi schädliche Radikale entstehen können, die ständig repariert werden müssen am Augenhintergrund, also das, was dort anfällt. Und auch da gibt es tatsächlich Untersuchungen wie groß ist der Einfluss von Sonnenlicht auf die Makuladegeneration? Und wenn ich dort eine gewisse Disposition habe, ist es sicher in einem späteren Stadium dann wieder günstig. Vielleicht einen gewissen UV Schutz in die Brille mitzutragen. Einfach um jetzt dieses Aggressivere Licht, was dann irgendwann schädlich werden könnte für die Zellen in einem späten Zeitraum, wo man das eben einfach ein bisschen mit abfangen kann.
Karen Teßmer: Macht die Lichtsituation, in der Sie sich bewegen, jetzt vielleicht in Ihrem Fall als Betroffene denn eigentlich einen großen Unterschied? Oder wissen Sie da was aus den Interaktionen mit anderen Betroffenen? Ob das für Betroffene große Unterschiede macht? In welchem Licht man sich bewegt?
Ruth Forschbach: Ja, also ich kann jetzt als hochgradig Kurzsichtige mit den Netzhautschäden, die ich habe, eindeutig sagen, das haben Sie vielleicht eben auch schon gemerkt, ich brauche Licht. Je, sage ich mal, je älter meine Netzhaut wird, Fortgeschrittener Jugend, Das wird natürlich nicht besser. Also ich brauche definitiv mehr Licht in Innenräumen. Wenn ich mich jetzt draußen bewege, ist es ein Problem wiederum für mich, weil die Sonne, die ich ja vom Grundsatz her mag, mich sehr blendet, ich aber wiederum keine normale Sonnenbrille tragen kann, weil das, was ich gerade wieder gesagt habe, das schränkt wiederum mein Sehen ein. Also ich habe ja ein schlechtes Kontrastsehen. So, also deshalb Kantenfilter sind glaube ich heute auch schon mal gefallen. Kantenfilterbrillen auch für die hochgradig Kurzsichtigen, weil die machen dann einfach diesen Seheindruck noch mal klarer, noch mal stärker. Muss dann aber auch probiert werden. Gibt ja gelb, braun, grün, alle möglichen Farben der Welt sozusagen. Also schön ausprobieren, das hilft tatsächlich.
Karen Teßmer: Und wie ist das eigentlich? Durch diese Kurzsichtigkeit hat man dann noch viele andere Symptome. Also ich weiß nicht, führt das zu Kopfschmerzen oder zu Desorientierung oder gibt es da noch andere Faktoren?
Ruth Forschbach: Bei mir mir nicht, auch nicht bei den Menschen, mit denen ich gesprochen habe, was ein Problem ist, ist ganz einfach mein einäugiges Sehen oder Menschen, die das eben erlitten haben. Mit meinem linken Auge habe ich ja noch einen sehr guten Seheindruck, also 0,60-0,65, je nachdem wie ich gefuselt bin, Sagt man im Rheinland, Also wie ich jetzt im Leben stehe. Ja, das ist, finde ich beachtlich. Ich habe ja noch nie 100 % gehabt. Also ich weiß gar nicht, wie das ist, deshalb freue ich mich darüber. Ja, aber auf dem anderen Auge sagte ich ja auch 0,15 und dann eben Mitte ist zentrales Sehen nix mehr. Und das ist natürlich sehr, sehr nicht gerade glücklich. Und das verursacht Kopfschmerzen, Das verursacht verschwommenes Sehen. Nicht immer, jeden Tag. Aber es kommt auch darauf an, wie bin ich gesettelt in mir. Das kann schon unglücklich machen. Ja, also nicht ganzen Tag, aber schon mal minutenweise.
Karen Teßmer: Glaube ich gern.
Stephan Wiegand : Ja, ich habe noch eine Frage eingesammelt: Führen Fettablagerungen im Auge auch zu Ablagerungen im Gehirn? Ist da ein adäquates Zusammenspiel beobachtbar oder zumindest in Studien das eine oder andere Mal zu belegen?
Dirk Sandner: Gute Frage.
Stephan Wiegand : Ja, das ist ist der Reiz der Fragen aus dem Publikum.
Dirk Sandner: Es ist sicher so, dass eine schlechte Ernährung, das wissen wir, Übergewicht ein Risikofaktor für die Entstehung einer Makuladegeneration ist. Beider Formen und lässt sich am Auge sehen wir Veränderungen mit diesen Ablagerungen jetzt draußen, was wir am Augenhintergrund sehen und die gleiche Konstellation habe ich an anderen Gefäßen und habe das auch an Veränderungen im Gefäßsystem. Es gibt aber nicht irgendwelche Fettablagerungen jetzt, die vergleichbar sind mit dem, was wir am Augenhintergrund sehen, im Gehirn, aber letztlich, dass ich in dieser Gesamtkonstellation sicher auch meine Durchblutungssituation im Gehirn verschlechtere, damit vielleicht auch was Merkfähigkeit angeht, dort einen gewissen negativen Effekt induzieren kann über einen gewissen Zeitraum das schon, aber wir sehen jetzt nicht dort quasi auch Dosenablagerungen oder ähnliches, wie wir es am Auge sehen, wo wir sagen können ja, das ist eins zu eins das, was wir im Auge haben, nur an einer anderen Stelle, das nicht.
Karen Teßmer: Das heißt, die Dosen sind sehr unspezifisch.
Dirk Sandner: Ja, mehr oder weniger, weil das eben einfach dort im retinalen Pigmentepithel Abbauprodukte, quasi aus dem Sehzyklus. Es ist eine relativ spezifische Dinge, die dort quasi nur am Auge sich abspielen.
Stephan Wiegand : Eine weitere Frage, die uns erreicht hat: Wenn man an Studien teilnehmen möchte, wohin sollte man sich da wenden? Gibt es eine Zentrale, wo man sich hinwenden kann? Wird man da gezielt angesprochen? Sucht einen da jemand aus nach einem Zufallsprinzip oder wie funktioniert das für die Patienten, genau an dieser Stelle teilnehmen zu können?
Dirk Sandner: Ja, also es ist sicher immer regional unterschiedlich. Für Dresden, für unsere Augenklinik kann ich sagen, dass wir jetzt eine Homepage haben, wo wir jetzt eben auch Projekte, wo wir vielleicht Patienten suchen, eben dort dann auch veröffentlichen würden. Wenn ich jetzt nicht genau weiß, ist eine Anfrage über das Sekretariat. Ich habe die und die Erkrankung läuft an ihrem Zentrum gerade eine Studie in der Richtung. Also das ist eine Möglichkeit. Wir selber gucken natürlich, wenn wir an Projekten teilnehmen bei unseren Patienten, die täglich sich vorstellen, welcher Patient könnte infrage kommen und würden sie dann direkt ansprechen. Also das wäre sozusagen der umgekehrte Weg. Sicher, wer das Internet nutzt, kann gucken, welche Studien sich auch über PRO-RETINA dort werden auch jetzt aktuell laufende Studien veröffentlicht werden. Und dann gucke ich nicht jede Klinik nimmt an jeder Studie teil. Dann gibt es immer so fünf, sechs Zentren und dann muss man gucken, welches wäre denn das nächste Zentrum jetzt für diese Art der Erkrankung, wo ich vielleicht infrage kommen würde? Und dann würde ich quasi die Klinik, wo das Zentrum ist, dort anschreiben und würde fragen Wie sieht das aus? Bis wann wird eingeschlossen? Wie sind die Kriterien? Kann ich mich mal vorstellen. Und meistens gibt es an den Kliniken wie gesagt eine Studienambulanz.
Stephan Wiegand : (...) Es ist jedes Mal wie eine Studie. Eine weitere Frage ist.
Ruth Forschbach: Ich. Ich würde gern noch was zu den Studien sagen.
Stephan Wiegand : Entschuldigung. Entschuldigung.
Ruth Forschbach: Und zwar die PRO-RETINA Deutschland verfügt über ein Patientenregister, liebe Damen und Herren, da können Sie sich daran beteiligen. Sie können an die PRO-RETINA schreiben oder auch anrufen. Und Ihre Angaben werden natürlich wirklich verschlüsselt. Sie müssen keine Sorge haben, dass die irgendwie weiß ich was zu irgendwelchen Studienzwecken durch die Gegend geschoben werden, sondern wenn dann Anfragen von den Kliniken kommen, dann werden Sie wiederum angefragt, ob sie an einer Studie teilnehmen möchten. Das heißt also nutzen Sie die Chance, Wir haben ein Patientenregister.
Stephan Wiegand : Okay, wir kommen zur nächsten Frage und die heißt Aufklärung an Schulen, Prävention. Gibt es eine Möglichkeit, dass man Eltern ein bisschen sensibilisiert, dass sie aufpassen, wenn eine Kurzsichtigkeit auftritt? Wenn man merkt, dass mit den Augen, mit dem Sehen etwas nicht hinhaut?
Ruth Forschbach: Ja.
Stephan Wiegand : Schön.
Ruth Forschbach: Wir vom Arbeitskreis haben einen Flyer gestaltet, natürlich mit unseren medizinischen Fachexperten. Und zwar ist das ein Merkblatt für Eltern, was natürlich genauso gut für Erzieher, für Großeltern, für Menschen, die sich mit Kindern beschäftigen. Dann gibt es bei der PRO-RETINA seit zwei Jahren ein sogenanntes Schulprojekt. Das hat eigentlich damit begonnen, dass man Schüler der höheren Klassen sensibilisieren wollte. Wie gehen Sie mit schwer sehbehinderten Menschen um oder gar mit blinden Menschen? Und packe ich die einfach mal am Arm und zerre sie über die Straße oder wie mache ich das? Und dann ist uns vom Arbeitskreis die Idee gekommen, wir könnten doch wunderbar eben auch die Myopie-Prävention darüber vermitteln. Und dieses Projekt ist jetzt seit einem halben Jahr gestartet und das wollen wir vermehrt auch in die Schulen tragen.
Stephan Wiegand : Großartig. Und das ist vielleicht auch eine Möglichkeit, diesen Podcast den Leuten mal zur Verfügung zu stellen. Dass sich vielleicht die eine oder andere Frage dadurch beantworten lässt. Letzte Frage Ich habe noch eine private Frage, also eine Frage. Jetzt ist die letzte aus dem Publikum und das ist Sonnenbrillen. Ab welchem Alter sind die sinnvoll? Gibt es da eine Faustregel? Gibt es da Erfahrungswerte?
Dirk Sandner: Es gibt keine Empfehlung, wenn ich das Gefühl habe, das ist für mich zu hell, ich komme damit gut zurecht. Man macht damit keinen Schaden. Es gibt keine generelle Empfehlung.
Stephan Wiegand : Okay, gestern habe ich einen Zeitungsartikel gefunden und habe den Herrn Professor Ader gleich zugeschickt. Da war nämlich die Meldung, dass ein Auge transplantiert wurde, komplett. Da habe ich mich dann gefragt zulaufend auf den heutigen Tag, wenn es solche Ansätze gibt und wenn es diese Möglichkeit gibt, wäre das auch etwas bei Makuladegeneration, so eine Transplantation und vielleicht auch teilweise Transplantationen irgendwie vorzunehmen oder ja ganze Augen zu transplantieren, das wird sicherlich nicht in den nächsten Tagen und Wochen die Regel werden. Und braucht man auch Spender dazu. Aber ist diese Form dieser Organtransplantation irgendwie eine Möglichkeit, die man realistisch verfolgen kann?
Dirk Sandner: Ich habe letztlich die Meldung auch gehört und ich habe mich, das ist ja glaube ich schon ein bisschen zurückliegend, wo das gemacht wurde bei einem Patienten, der verunfallt war, also wo jetzt nicht nur das Auge kaputt war, sondern auch quasi die gesamte Umgebung mit zerstört war. Und bisher war ich eigentlich davon ausgegangen, dass das quasi als funktionelles Konzept nicht funktioniert, weil man sich ja vorstellen muss, quasi das Auge nimmt die Information auf und das Kabel leitet dann die Information weiter zum Gehirn. Und wenn ich das Auge komplett ersetze, dann gehe ich auch davon aus, dass das Kabel ja irgendwo unterbrochen oder gekappt werden muss. Und dann muss ich das Kabel vom transplantierten Auge mit dem Kabel vom …
Stephan Wiegand : Vom Gehirn.
Dirk Sandner: Vom Gehirn zusammennähen und diese Informationsbarriere, die dort an dieser Schnittstelle entsteht, die war für mich bisher ein NoGo, dass dort irgendwo Informationen weitergegeben werden kann. Jetzt ist die Frage kann sich das Ganze regenerieren? Glaube ich eher nicht. Ist das Ganze nur ein kosmetischer Aspekt, den ich dort umsetze, dass ich sage okay, ich habe zwar ein Auge, aber ich habe jetzt kein funktionelles Auge. Deswegen machen wir ja quasi diese Teilschritte, weil wir versuchen, einzelne Zellkomponenten, die irgendwo Kontakt finden können, die versuchen wir zu ersetzen. Das Ganze funktioniert nach meiner Kenntnis bisher nicht. Ich weiß ja nicht, ob da…
Stephan Wiegand : Okay, also keine funktionelle Transplantation, sondern rein aus ästhetischen Gesichtspunkten.
Dirk Sandner: Die ganzen Nervenfasern müssten quasi von dem transplantierten Auge wieder in Richtung Gehirn wachsen und müssten dort raus.
Stephan Wiegand : Das ist mir schon klar. Okidoki, vielen, vielen Dank! Das waren die Fragen aus dem Publikum. Wir können sicher noch kurz fortführen in der Runde. Vielen herzlichen Dank.
Karen Teßmer: (...) Bei der Gelegenheit auch noch mal vielen Dank an die Band. Ich fand es ganz fantastisch. Danke schön.
Stephan Wiegand : Patrick Neumann und Jo Aldinger.
Ruth Forschbach: Dann auf Wiedersehen und vielen Dank.
Give us your feedback - simply, quickly and anonymously.
Here are a few impressions of our event.

Organisator Stephan Wiegand © André Wirsig

Musikalische Unterstützung durch Jo Aldinger (rechts) und Patrick Neumann (links) © André Wirsig

© André Wirsig

© André Wirsig

Moderatorin Karen Teßmer © André Wirsig

Referent Mike O. Karl © André Wirsig

Referent Mike O. Karl © André Wirsig

Referent Thomas Ach © André Wirsig

Referent Thomas Ach © André Wirsig

© André Wirsig

Referent Mike O. Karl © André Wirsig

© André Wirsig

© André Wirsig
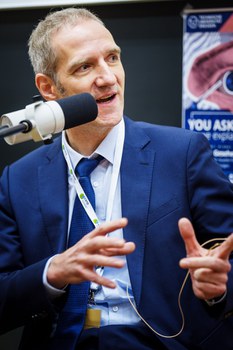
Referent Dirk Sander © André Wirsig

Referent Dirk Sander © André Wirsig

Referentin Ruth Forschbach © André Wirsig

Referentin Ruth Forschbach © André Wirsig

© André Wirsig

Moderatorin Karen Teßmer © André Wirsig

© André Wirsig

© André Wirsig

© André Wirsig

Organisator Stephan Wiegand (links) und Referent Thomas Ach (rechts) © André Wirsig

© André Wirsig

© André Wirsig

Musikalische Unterstützung durch Jo Aldinger © André Wirsig

© André Wirsig

Organisatorin Doreen Pretze im Gespräch mit einer Patientin © André Wirsig

Gastgeber Marius Ader © André Wirsig
When: November 11, 2023, 2:00 - 3:00 pm
Where: Center for Regenerative Therapies Dresden (CRTD) (Fetscherstraße 105)
Our Advisors:
- PD Dr. Thomas Ach - FEBO, Senior Consultant, Deputy Clinic Director of the University Eye Clinic Bonn
- Prof. Mike O. Karl - Professor for Stem Cell Research and Neurogenesis of the Retina, C-Center for Regenerative Therapies Dresden (CRTD), German Center for Neurodegenerative Diseases Dresden (DZNE)
- Ruth Forschbach - Member of PRO RETINA Deutschland e. V.
- Dr. med. Dirk Sander - Senior Consultant at the Clinic and Polyclinic for Ophthalmology,
Carl Gustav Carus University Hospital at the TU Dresden
Moderator: Dr. Karen Teßmer, Postdoc, Ader AG, Center for Regenerative Therapies Dresden (CRTD)
This project is funded by the Federal Ministry of Education
Research (BMBF) and the Free State of Saxony as part of the Excellence Strategy of the
Federal and State governments.






























