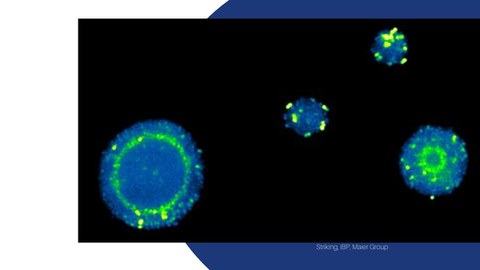
Kollektive Dynamik des Membranpotentials in bakteriellen Kolonien
- Prof Dr Berenike Maier Universität zu Köln, Mathematisch-Naturwissenschaftliche Fakultät, Institut für Biologische Physik.
Strukturierte Populationen von Bacillus subtilis koordinieren mittels elektrischer Kommunikation ihren Metabolismus. Derzeit ist unklar, ob andere bakterielle Spezies ebenfalls ihr elektrochemisches Verhalten synchronisieren. Wir haben herausgefunden, dass kugelförmige Kolonien, die durch Neisseria gonorrhoeae gebildet werden, im Zentrum hyperpolarisieren. Eine kugelförmige Welle von hyperpolarisierten Bakterien wandert anschließend radial nach außen. Die Hyperpolarisation ist gefolgt von einer Depolarisation der Bakterien im Zentrum. Dieser Antrag verfolgt das Ziel, Auslöser der Hyperpolarisation zu finden, den Mechanismus der Ausbreitung der Hyperpolarisation innerhalb der Kolonie zu verstehen sowie den Zusammenhang zwischen Membranpotential und Wachstumsinhibition und dessen Auswirkung auf die Fitness der Gesamtpopulation zu untersuchen. Insbesondere, werden wir Wachstumsinhibierung im Zentrum der Kolonie mit der Dynamik des Membranpotentials korrelieren. Hierzu kombinieren wir unsere kürzlich entwickelte Methode für die räumlich und zeitlich aufgelöste Messung von Wachstumsraten mit Werkzeugen für die Charakterisierung des Membranpotentials. Im nächsten Schritt werden wir zwei mögliche Auslöser für die Hyperpolarisation untersuchen. Zum einen werden wir uns auf die Verarmung von Sauerstoff und Nährstoffen konzentrieren. Zum anderen werden wir testen, ob der Aufbau des mechanischen Drucks im Zentrum der Kolonie das Wachstum limitiert und die Hyperpolarisation auslöst. Hierzu werden wir den Druck variieren, indem wir die anziehenden Wechselwirkungskräfte zwischen den Bakterien verändern. Diese Veränderungen werden durch verschiedene genetische Modifikationen von Typ 4 Pili bewirkt und mittels Laserfallen charakterisiert. Schließlich werden wir der Frage nachgehen, ob interzelluläre Kommunikation für die Ausbreitung der Hyperpolarisation notwendig ist. Hierzu werden wir die räumlich-zeitliche Dynamik der Hyperpolarisation in Kolonien mit unterschiedlichen Strukturen untersuchen. Auf lange Sicht wird es wichtig sein, die Ionenkanäle zu identifizieren, die für die Hyperpolarisation verantwortlich sind und die Fitness-Effekte der kollektiven Membran-Potential Dynamik zu verstehen.
| Researcher(s) |
|
Paul Schiefer (PhD Student) |
Über uns
Wir sind eine multidisziplinäre Gruppe, in der Physiker, Biologen und Biochemiker eng zusammenarbeiten und eine Kombination von Werkzeugen aus der Nanotechnologie, Bildanalyse, Molekularbiologie und Genomik einsetzen. Unser Schwerpunkt liegt auf der Physik von bakteriellen Systemen. Auf der Ebene einzelner Moleküle untersuchen wir den Mechanismus der Krafterzeugung in Bakterien.
- Wie bestimmen die interbakteriellen Kräfte die Struktur von Biofilmen?
Forschungsschwerpunkt
besonders an bakteriellen Motoren interessiert, die an der Motilität und dem horizontalen Gentransfer beteiligt sind. Wir untersuchen die evolutionäre Bedeutung dieser molekularen Motoren auf der Ebene der Populationen.
- Was sind die Kosten und Vorteile des horizontalen Gentransfers?
- Wie entwickeln sich die Interaktionskräfte in Biofilmen?
Kontaktieren Sie uns
Universität zu Köln
Email: berenike.maier@uni-koeln.de