28.09.2021
Nachwachsende Rohstoffe: Von Krabben zu Solarzellen und was mit Chitin sonst noch funktioniert
Käfer, Fliegen, Libellen, Krebse, andere Arthropoden, bestimmte weitere Tiere und Flechten haben unter anderem eins gemeinsam: sie sind mit einer faszinierenden Substanz bedeckt, von der sie Unmengen (mindestens Hunderte Mio. t jedes Jahr) produzieren: Chitin, das nach Cellulose häufigste Biopolymer überhaupt.
Chitin fällt z.B. beim Krabbenpulen in beträchtlichen Mengen an und ist damit ein nachwachsender Rohstoff, thermisch (bis fast 300°C) und mechanisch viel robuster als andere wie Holz, Seide oder andere Proteine, dazu auch in bestimmten Medien löslich und damit mit konventionellen Techniken zu verarbeiten, wenn man nicht das native Material einsetzen kann oder will.
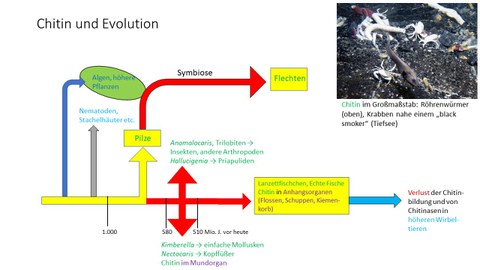
Es kommt außerdem in Mollusken einschließlich Kopffüßern, Pilzen, marinen Schwämmen und niederen Wirbeltieren (Kiemengerüste von Schleimaalen und Neunaugen, Flossenstrahlen und Schuppen von manchen Fischen) vor. Wie die Verteilung der Bildung und Nutzung von Chitin über die biologischen Taxa zeigt,
fängt die Geschichte/Funktionalität des Chitins in der biologischen Evolution nicht damit an, harte Schalen, Extremitäten (Beine, Flügel, Flossen) oder Mundwerkzeuge (Schnecken, Kalmare) zu bilden, sondern reicht viel weiter ins Präkambrium zurück, also in die Zeit vor mehr als 543 Millionen Jahren (die ersten Arthropoden und Kopffüßer lebten im mittleren Kambrium). Die molekulare Uhr (Vergleiche von DNA-Daten und Proteinsequenzen) zeigt, wann ungefähr sich die letzten gemeinsamen Vorfahren von Organismen mit bzw. ohne Chitin unter den Tieren und Pilzen von diesen und voneinander trennten: eben im Präkambrium vor 570 – 580 Mio. Jahren. Stellt sich also die Frage: was haben die damaligen Organismen (nicht nur oder noch nicht als Tiere einzustufen) eigentlich damit gemacht (die Biosynthese von Chitin ist ziemlich kompliziert) – Hartstrukturen daraus existieren erst seit maximal 530 Mio. Jahren? Dazu muss man sich natürlich die Stoffeigenschaften dieses Biopolymers genauer anschauen, etwa seine Affinität zu Metallionen. Ursprünglich wurde die Fähigkeit von Chitin, Metallionen oder Komplexe davon zu binden, zur Aufbereitung von Kernbrennstoffen (Muzzarelli et al. 1972; Chitin ist auch strahlenchemisch äußerst robust) oder zur Abtrennung von Schwermetallen aus Abwasserströmen oder Minenausläufen genutzt. Davon ausgehend ging ich zunächst (2013) daran, zu untersuchen, bis zu welchen Restkonzentrationen in Wasser (oder anderen Lösungsmitteln) hinunter die Adsorption funktioniert, um Chitinoberflächen als „Fallen“ für Kontaminanten in der Umweltanalytik zu verwenden. Die Mindestkonzentrationen, bis zu denen das Chitin tatsächlich Metalle bindet, sind teils extrem gering (außer für Alkalimetalle sowie Mg, Ca), wenige Nanogramm/l Wasser reichen für ein sicher erkennbares Signal. Mehr noch: bei passender Anordnung von Chitinproben in einem Wasserkörper (Bach, Teich, See) und direkt benachbartem Sediment (Ufer, Seeboden) ist an Hand der Konzentrationsverhältnisse verschiedener Elemente auf den beiderseits der Grenzfläche platzierten Chitinplättchen – aufgeklebt auf Objektträgern oder Plastikstreifen (10 min Expositionszeit reichen) – erkennbar, ob Metallionen im Sediment durch biochemische Aktivität (etwa Nickel in Methanbildnern) oder Fällungsreaktionen aufgenommen oder aber bei der Sulfatreduktion freigesetzt werden (Ba, Pb), so dass man ziemlich tief ins Sediment hineinschauen kann. Die Bindung einiger Elemente, wie von Chrom oder des Seltenerdmetalls Europium, von dem noch zu reden sein wird, hängt auch von deren Oxidationsstufe ab, d.h. dass sich nach chemischen, elektrochemischen oder photochemischen Redoxvorgängen die Bindung der betreffenden Elemente an Chitin bedeutend vermindert bzw. verstärkt.
Die Analyse der Messdaten an Chitin beinhaltet also sehr viele nicht offensichtliche Informationen, und der letztgenannte Effekt gibt uns die Möglichkeit, mit Chitin auch dahingehend zu spielen, dass man es zur direkten Umwandlung chemischer oder optischer Energie in elektrischen Strom nutzen kann, wenn man diese Sorptionsänderung in einem (langsamen) Flüssigkeitsstrom realisiert. Chitin als Komponente von Brennstoff- bzw. Solarzellen: das ist unsere Vision, und erste Schritte dazu sind bereits getan.
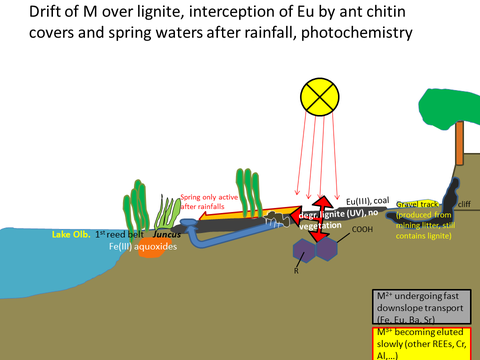
Chitin in biologischen Solarzellen: das gibt es offenbar auch in der Natur, in der von Albanien bis Tansania und Indien weit verbreiteten Hornissenart Vespa orientalis: Teile ihres Chitinpanzers (zwischen den Flügeln) und die Eierkokons zeigen bei Belichtung Photoströme und -spannungen. Wir haben also hier ein biologisches Vorbild (von dem wir allerdings erst lange nach Beginn unserer Experimente erfuhren), machen biomimetische Photochemie; das Chitin ist gleichartig, die aktive Komponente dagegen eine andere: Europiumsalze statt dem Molekül Xanthopterin, dessen Farbe jede:r etwa von Urin kennt, in den Hornissen. Eu(III) bleibt wie andere Seltenerdmetalle (Lanthanoiden) auch in Gegenwart von Komplexbildnern fest an Chitin sorbiert, selbst bei minimalen Umweltkonzentrationen, wie wir sie im Sickerwasser in Sediment und kleinen Quellen rings um den Olbersdorfer See gefunden haben (≤ 2 µg/l) oder bei Zusatz von Komplexbildnern (die Aminosäure Glycin steigert die Sorption von Eu an Chitin sogar). Das photochemisch durch Umsetzung/Abbau organischer Substanzen wie Alkoholen, Zuckern, Carbonsäuren, Pflanzenfetten wie Olivenöl und auch problematischen organischen Lösungsmitteln wie Toluol oder Chlorbenzol, sogar Braunkohle (die lokal in Olbersdorf vorfindliche Kohle ist in organischen Medien wie Dimethylformamid löslich!) gebildete Eu2+ dagegen wird ausgewaschen. Aus dem so aufgebauten Konzentrationsgradienten beider Oxidationsstufen resultiert eine elektrochemische Spannung. Analytik, Sensorik und Energieumwandlung (photoassistierte Brennstoffzellen, die nicht nur Wasserstoff sondern organische Substanz umsetzen) fließen hier ineinander.
Bei Ameisen ließen sich durch schrittweise Analytik (zunächst Auflösen der wachsartigen Cuticula, dann der äußeren Chitinschichten, schließlich des Restes der Ameise mit je separater Elementanalytik) Elementaufnahmen über den Chitinpanzer, also Bodenkontakt, von solchen unterscheiden, die oral mit Beutetieren oder Trinkwasser erfolgt waren. Chemisch ähnliche Elemente gehen dabei oft verschiedene Wege, etwa Zink und Cadmium oder Europium (bindet anomal gut an Chitin) und andere Lanthanoiden… Diese breite, bis auf K, Mg und Ca auch alle essentiellen Metalle umfassende Sorptionswirkung könnte – so unsere These – auch die ursprüngliche biologische Funktion von Chitin gewesen sein. Ins Sediment gedrückte „Anhängsel“ – aus Chitin bestehend, hart, und damit Vorläufer von Beißorganen oder Beinen – nahmen schnell essentielle Spurenelemente auf, die dann unter leichter Säureeinwirkung (die Bindung von Metallen an Chitin sinkt mit fallendem pH) abgeleckt werden konnten. Mindestens ein fossil überlieferter Vorläufer mit Chitin bedeckter Tiere (Hallucigenia sparsa/Priapuliden) hat einen diesbezüglich vielsagenden Körperbau...
Für die nächsten Schritte unserer Forschung hoffen wir auf Förderung auch durch die DFG. Der Schwerpunkt liegt hier auf der Umweltsensorik. Der Antrag ist eingereicht, und näher Interessierte seien auf unsere dieser Tage online gestellte Publikation über Chitin und dessen evolutionäre Bedeutung und Anwendungsperspektiven in MDPI Polysaccharides verwiesen.
Prof. Dr. Stefan Fränzle ist außerplanmäßiger Professor an der Professur für Umweltbiotechnologie des IHI Zittau. Am IHI Zittau wirkt er seit 2001.