Forschungsfelder
Unsere Hauptforschungsfelder sind die optische Kohärenztomografie , die Spektroskopie/multimodale Bildgebung und die Thermografie. Erfahren Sie hier mehr zu diesen drei Themen!
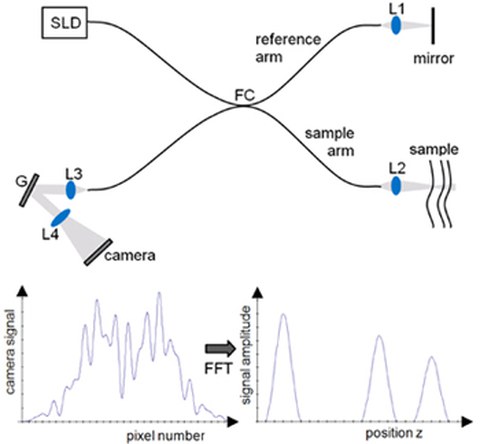
Schematische Darstellung eines Fourier Domain OCT Systems.
Optische Kohärenztomografie (OCT)
Der Begriff Optische Kohärenztomografie (engl. optical coherence tomography – OCT) wurde erstmals 1991 in der Arbeit von Huang und Fujimoto aufgeführt. Die OCT ist eine nicht-invasive, kontaktlose Methode zur Bildgebung in streuenden Medien bis in eine Tiefe von etwa 1 mm mit einer Auflösung im Bereich zwischen 1 und 15 µm. Die OCT basiert auf der Weißlichtinterferometrie und misst die Amplitude des rückgestreuten Lichtes als Funktion des optischen Weges. Anwendungsgebiete der OCT sind sowohl in der biomedizinischen Forschung als auch der klinischen Praxis zu finden. Weiterhin findet die OCT auch immer mehr Anwendungen im industriellen Umfeld, insbesondere in der zerstörungsfreien Materialanalyse.
Die von uns entwickelten und selbst aufgebauten OCT-Systeme basieren alle auf dem Verfahren der Fourier Domain OCT (FD OCT), bei dem das entstandene Interferenzsignal zunächst spektral zerlegt und die Tiefeninformation dann aus dem gesamten Interferenzspektrum gewonnen wird. Die Technik wird fortwährend von uns weiterentwickelt, um die Auflösung und die Eindringtiefe in das zu untersuchende Medium zu verbessern und die Aufnahmegeschwindigkeit zu steigern. Außerdem werden in Zusammenarbeit mit verschiedenen Bereichen an der Medizinischen Fakultät und dem Universitätsklinikum Carl Gustav Carus unterschiedliche Scanköpfe entwickelt und erprobt.
Spektroskopie und multimodale Bildgebung
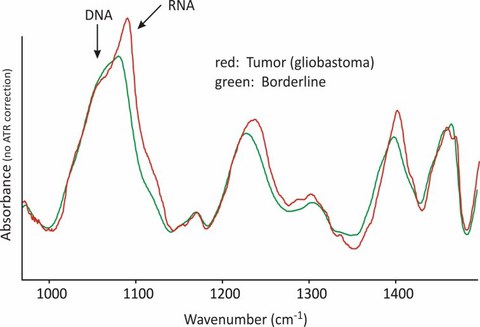
Infrarotspektren von nativem, normalem (Tumorgrenze) und tumorösem Gewebe. Deutliche Unterschiede zeigen sich im Bereich der RNA-Banden.
Die optische Molekülspektroskopie mit ihren beiden wichtigsten Vertretern, der Infrarot- und Raman-Spektroskopie, gilt nach wie vor als die Methode mit dem höchsten Informationsgehalt zur molekularen Struktur. Sie lässt Eigenschaften, die auf strukturellen Merkmalen der Probe beruhen, auf molekularem Niveau ohne zusätzliche Marker erkennen. Damit unterscheidet sie sich grundlegend von mikroskopischen Untersuchungsmethoden und Markierungsmethoden. Während die Raman-Spektroskopie vor allem Potenzial für in situ Anwendungen besitzt, wird die Fourier-Transform-Infrarot (FT-IR) Spektroskopie hauptsächlich zur ex vivo Untersuchung von Gewebe und Zellen eingesetzt. Das Anwendungspotenzial hat sich dabei mit der Bereitstellung von Arraydetektoren erheblich vergrößert. Mittels FT-IR Imaging Spektroskopie ist es möglich, die räumliche Verteilung chemischer Merkmale innerhalb einer Schicht zu bestimmen. Daneben erlauben Methoden der nichtlinearen Raman-Spektroskopie eine schnelle bildliche Darstellung von Gewebe und Zellen. In Kombination mit weiteren optischen Bildmodalitäten lassen sich völlig neue Einblicke in die Chemomorphologie und Funktion von biologischem Material gewinnen. Ein Schwerpunkt der Arbeiten nimmt dabei die histologische Charakterisierung von Tumoren während der operativen Therapie ein.
Die gegenwärtige Ausrichtung mit Bezug zu medizinischen Fragestellungen betrifft u. a. folgende schwerpunktmäßige Arbeitsgebiete:
- Bildgebende nichtlineare Raman-Spektroskopie in der Neurochirurgie und regenerativen Medizin
- In situ FT-IR Spektroskopie in der Neurochirurgie
- In situ Raman-Spektroskopie von Tumormodellen an lebenden Mäusen
- Spektroskopische Differenzierung von neuralen Zellen
- Untersuchung von Knochengewebe
- Untersuchungen zur Kollagenvernetzung der Cornea
- In ovo Geschlechtsbestimmung des Hühnereies
Thermografie
Bildgebende Verfahren haben eine immense Bedeutung für die klinische Diagnostik. Dabei sind die Techniken besonders interessant, welche Informationen bereitstellen, die außerhalb des visuellen spektralen Bereiches liegen (Violett 380 nm bis Rot 780 nm Wellenlänge) und damit mit normalen Weißlichtkameras oder dem menschlichen Auge nicht wahrnehmbar sind. So zeigen z. B. MRT und CT den inneren Aufbau des Körpers unter Ausnutzung der Wechselwirkung starker magnetischer Felder (MRT) bzw. hochenergetischer Strahlung (CT/Röntgen) mit biologischem Gewebe. Zu dem nicht sichtbaren Spektralbereich gehört auch Wärmestrahlung (Infrarotstrahlung von 780 nm bis 50 µm Wellenlänge) die von jedem Gegenstand emittiert wird. Diese Wärmestrahlung ist für herkömmliche Kamerasystem nicht sichtbar und die darin enthaltenen Information, wie Wärmeverteilung und Wärmetransport an der Oberfläche eines Körpers, kann nicht erfasst und genutzt werden. Durch Verwendung von Thermografiesystemen mit entsprechenden optischen Linsen und Detektoren kann die Wärmestrahlung eines Objektes und die zeitliche Änderung sichtbar gemacht werden (z. B. Wärmedämmungsuntersuchung an Gebäuden).
Für die medizinische Diagnostik ergibt sich daraus ein enormes Potential, da biologisches Gewebe, abhängig von seiner Zellzusammensetzung und Funktion, einen unterschiedlichen Stoffwechsel und damit einen differenzierten Wärmeumsatz aufweist. Mit hoch sensitiven Kameras können Temperaturunterschiede von wenigen Millikelvin lokal aufgelöst erfasst werden, womit die Darstellung kleinster Unterschiede in der Durchblutung und Aktivität von Gewebebereichen möglich wird.
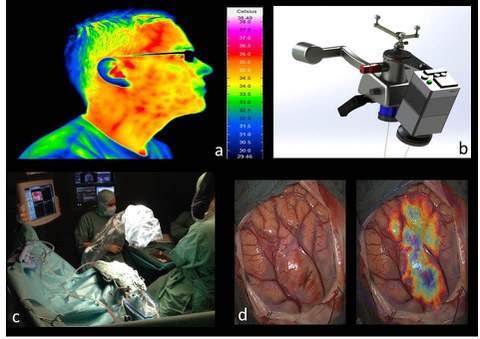
Thermografie in der Neurochirugie. Mittels geeigneter Detektoren und Optiken lässt sich die Wärmestrahlung eines Objektes (im Wellenlängenbereich von 7 bis 14 µm) darstellen und zeitliche Änderungen der Wärmeverteilung erfassen (a). Über einen speziellen Adapter lässt sich die Thermografiekamera an ein Operationsmikroskop anschließen und während neurochirurgischer Eingriffe wie Tumorentfernung, Epilepsiebehandlung oder Aneurysmenversorgung anwenden (b und c). Ziel ist die intraoperative Auswertung der erfassten Thermogramme, um pathologische Veränderungen in der Wärmeverteilung des Hirngewebes zu erkennen und diese Informationen dem Operateur während des Eingriffes bereitzustellen (d).
In Kooperation mit der Klinik für Neurochirurgie des Uniklinikums Dresden wird eine Methode entwickelt, um über die Auswertung der zeitlichen Erfassung der Wärmeverteilung Aussagen über die Lokalisation verschiedener Gewebearten im menschlichen Gehirn zu ermöglichen. Da momentan intraoperativ wenige Möglichkeiten bestehen veränderte Gewebestrukturen differenziert zu diagnostizieren, stellt die Thermografie eine vielversprechende Methode zur Verbesserung der Patientenversorgung bei neurochirurgischen Eingriffen dar. Im Rahmen des Projektes wird untersucht wie sich die Wärmeverteilung von pathologischem Gewebe (z. B. Tumore) von gesundem Gewebe unterscheiden lässt, wie die Durchblutung von Gewebeabschnitten und Durchblutungsstörungen thermografisch erfasst werden können und welche Möglichkeiten zur Lokalisierung von funktionellen Hirnrealen (sensorische, motorische und assoziative Bereiche) bestehen.
