Mar 03, 2026
New Insights into Radiation Protection: The Effects of Americium and Decorporation Agents on kidney cells
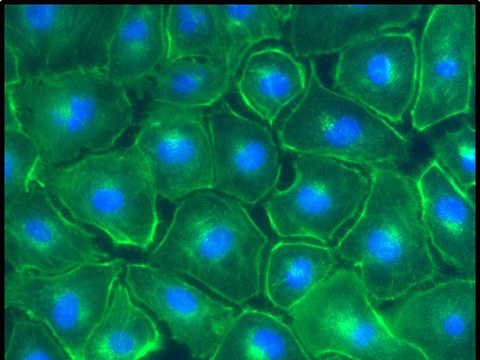
Fluorescence microscope image of kidney cells after americium uptake.
An interdisciplinary research team at TUD Dresden University of Technology has, for the first time, investigated the effects of the radioactive elements americium and curium, as well as the decorporation agents DTPA and LIHOPO, on kidney cells. The results provide important impulses for the development of new therapies following the incorporation of radioactive substances and for advancing radiation protection strategies. The study by the Central Radionuclide Laboratory at TUD was recently published in the journal ‘Ecotoxicology and Environmental Safety’.
Americium and curium are byproducts of the nuclear fuel cycle and may be released into the environment in cases of improper handling or accidents. If they enter the human body through the consumption of contaminated food, these elements accumulate in the liver, bones, and kidneys. In these organs, both elements act not only as chemical toxins, but also as radiotoxic elements due to the ionizing radiation they emit. So-called decontamination agents are used for treatment, which bind these radionuclides and thus facilitate their excretion.
In the current study, the researchers investigated how the radioactive nuclide 243Am (americium) reacts with rat kidney cells in the laboratory. They also tested how two special decontamination agents CaNa₃-DTPA and 3,4,3-LI(1,2-HOPO) can help remove the substance from the body. The active ingredient LIHOPO is considered a particularly promising candidate for future treatment.
Chemotoxicity and Radiotoxicity Analyzed Separately for the First Time
The results show that americium severely damages kidney cells. The cells were significantly less viable and their structure changed visibly. Oxidative stress occurred, caspases were activated (a sign of programmed cell death) and there were more DNA double-strand breaks. For the first time, the proportion of the radiation dose was measured separately from the chemical toxicity. Dr Thomas Kormoll's Radiation Physics Working Group at the Institute of Nuclear and Particle Physics analysed the radiation dose of americium in a microdosimetric model. The analysis showed that under the experimental conditions, most of the radiation dose came from the americium in the surrounding medium, not from that in the cells.
“Our data allows us to take a differentiated look at the chemotoxic and radiotoxic effects of americium on kidney cells for the first time,” explains lead author Dr Anne Heller, former research assistant at the Chair of Radiochemistry and Radioecology at TUD. “In particular, the high significance of α-radiation from extracellular americium and the low contribution of intracellular americium had neither been proven nor expected until now.” Dr Thomas Kormoll adds: “In this work, we succeeded for the first time in completely closing the circle from physical dosimetry at the cellular level to external reference irradiations and cellular effects. This comprehensive link offers numerous starting points for gaining further fundamental data and deepening our understanding of the effects of radiation at the cellular level.”
Decorporation Agents with very different Biological Profiles
A key finding of the study is the comparison of the two decorporation agents. DTPA binds americium in such a way that the resulting complexes hardly enter the cells. As a result, less americium is absorbed and the cells suffer significantly less biochemical damage. LIHOPO behaves differently: it forms complexes that penetrate the cells well. Under laboratory conditions, this led to higher americium uptake and thus to greater chemical cell damage. However, this also suggests that these complexes in the body – where conditions are different – could possibly escape from the cells again and be transported away via the blood.
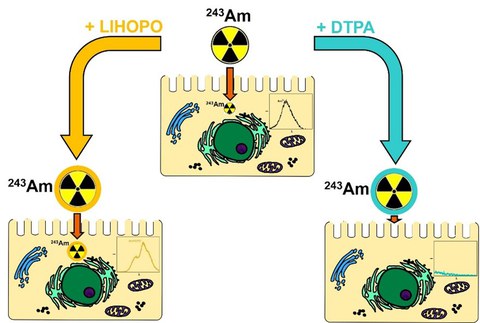
Figure 1: Schematic representation of the contrasting effects of the decorporation agents DTPA and LIHOPO on intracellular americium uptake in renal cells under stationary in vitro cell culture conditions.
"These findings provide a possible explanation for LIHOPO's superior performance compared to DTPA in preclinical studies: LIHOPO has the potential to remobilise americium already stored in cells, whereas DTPA can only bind americium circulating in the bloodstream," explains Christian Senwitz, former PhD student at the Chair of Radiochemistry/Radioecology at TUD. At the same time, the results make it clear that high complex stability alone is not a sufficient criterion for therapeutic efficacy
Relevance for Radiation Protection and Clinical Research
The study closes a significant knowledge gap regarding the cellular effects of americium and curium, particularly with regard to the kidney as a relevant target organ. It provides an important basis for evaluating decontamination strategies and underscores the need to consider molecular binding forms, cellular transport mechanisms and radiation exposure together.
The research was conducted in close collaboration between scientists from the Central Radionuclide Laboratory of the Radiation Protection Division, the Chair of Radiochemistry/Radioecology, the Radiation Physics Group at the Institute of Nuclear and Particle Physics at TUD, and the Institute of Resource Ecology at the Helmholtz-Zentrum Dresden-Rossendorf (HZDR).
Publication
Heller, A. and Senwitz, C. et al. (2025): Am/Cm(III) and DTPA/LIHOPO interactions with renal cells in vitro studied by bioassays, luminescence spectroscopy, and microdosimetry. Ecotoxicology and Environmental Safety 307, 119445. https://doi.org/10.1016/j.ecoenv.2025.119445
This research was part of the RADEKOR collaborative project funded by the German Federal Ministry of Research, Technology and Space (BMFTR) (FKZ 02NUK057B).
Contact:
Dr. Margret Acker
Central Radionuclide Laboratory
Tel. +49 351 463-32477
E-Mail:
Dr. Thomas Kormoll
Radiation Physics Group, Institute of Nuclear and Particle Physics
Tel. +49 351 463-33148
E-Mail:
