01.02.2022
Biofilme durchleuchtet: die Forschende entschlüsseln die Geheimnisse der Biofilme
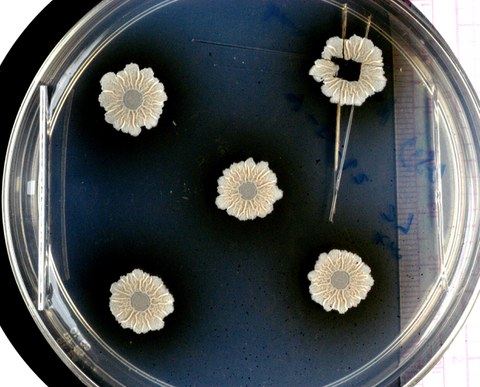
Wenn sich Bakterien zu Gemeinschaften zusammenschließen, können sie komplexe Strukturen bilden. Das Foto zeigt Biofilme aus dem Wildtyp Bacillus subtilis.
Die meisten Bakterien haben die Fähigkeit, sich zu Gemeinschaften zusammenzuschließen. Sie bilden Biofilme, die auf den unterschiedlichsten Oberflächen haften und schwer zu entfernen sind. Dies kann zu großen Problemen führen, zum Beispiel in Krankenhäusern oder in der Lebensmittelindustrie. Nun hat ein internationales Team unter Leitung der Hebrew University, Jerusalem, und der B CUBE an der TU Dresden ein Modellsystem für Biofilme untersucht und dabei herausgefunden, welche Rolle die Strukturen im Inneren des Biofilms bei der Verteilung von Nährstoffen und Wasser spielen.
Bakterielle Biofilme können auf fast allen Arten von Oberflächen gedeihen. Man kann sie auf Steinen und Pflanzen, auf Zähnen und Schleimhäuten finden, aber auch auf Kontaktlinsen, medizinischen Implantaten oder Kathetern, in den Schläuchen der Milchindustrie oder Trinkwasserleitungen, wo sie eine ernsthafte Gefahr für die menschliche Gesundheit darstellen können. Manche Biofilme sind auch nützlich, so sorgen bestimmte Biofilme bei der Herstellung von Käse nicht nur für die vielen winzigen Löcher, sondern auch für den kräftigen Geschmack.
Ein Gewebe mit Strukturen
„Biofilme sind nicht einfach nur eine Ansammlung von sehr vielen Bakterien, sondern ein Gewebe mit besonderen Strukturen", erklärt Prof. Liraz Chai von der Hebrew University in Jerusalem. Gemeinsam bilden die Bakterien eine Schutzschicht aus Kohlenhydraten und Proteinen, die so genannte extrazelluläre Matrix. Diese Matrix schützt die Bakterien vor Desinfektionsmitteln, UV-Strahlung oder Austrocknung und sorgt dafür, dass sich Biofilme nur schwer mechanisch entfernen oder chemisch abtöten lassen. Die Matrix ist jedoch kein homogener Schlamm. „Das ist ein bisschen wie in einem Pflanzenblatt, es gibt spezialisierte Strukturen, zum Beispiel Wasserkanäle und winzige Fältchen", sagt Chai.
Gemeinsam mit Prof. Yael Politi, Forschungsgruppenleiterin am B CUBE - Center for Molecular Bioengineering an der TU Dresden und Expertin für die Charakterisierung biologischer Materialien, setzte Prof. Chai die zerstörungsfreie Analysetechnik Röntgenbeugung ein, die an der Synchrotronstrahlungsquelle BESSY II am Helmholtz-Zentrum Berlin (HZB) verfügbar ist.
"Das Gute an dieser Technik und den Instrumenten ist, dass wir recht große Flächen abbilden können. Durch die Kombination von Röntgenbeugung und Fluoreszenz können wir nicht nur die molekularen Strukturen im Biofilm sehr genau analysieren, sondern gleichzeitig auch die Anreicherung bestimmter Metallionen, die im Biofilm transportiert werden, verfolgen und mehr über ihre biologische Rolle erfahren", erklärt Yael Politi.
Die Proben: Biofilme aus Bacillus subtilis
Als Proben verwendeten sie Biofilme aus Bacillus subtilis, einem harmlosen Bakterium, das auf Pflanzenwurzeln gedeiht und mit ihnen eine nützliche Symbiose eingeht. Der Biofilm speichert Wasser, so dass die Pflanze bei Trockenheit vermutlich aus dem Biofilm Feuchtigkeit entnehmen kann, außerdem schützt er die Wurzeln vor Krankheitserregern. Im Gegenzug ernähren sich die Zellen im Biofilm von Wurzelexsudaten. Gleichzeitig sind die Biofilme aus diesem Bakterientyp ein Modellsystem, das für viele Biofilme stehen kann.
Strukturen beeinflussen den Transport von Metallionen
An der MySpot-Beamline von BESSY II untersuchten die beiden Expertinnen mit ihren Teams nun eine große Fläche (mm2) aus diesen Biofilmproben. Sie konnten die Strukturen innerhalb des Biofilms räumlich auflösen und gut zwischen Matrixkomponenten, Bakterienzellen, Sporen und Wasser unterscheiden. „Die Röntgenfluoreszenzspektroskopie ist eine Methode, mit der wir wichtige Metallionen wie Kalzium, Zink, Mangan und Eisen auch in Spuren nachweisen können", sagt Dr. Ivo Zizak, HZB-Physiker, der die MySpot-Beamline betreut. So konnte ein Zusammenhang zwischen der Morphologie des Biofilms und der Verteilung der Metallionen hergestellt werden.
Die Auswertung zeigt, dass sich Kalzium-Ionen bevorzugt in der Matrix ansammeln, während sich Zink-, Mangan- und Eisen-Ionen entlang der Falten anreichern, wo sie möglicherweise die Bildung von Sporen auslösen, die für die Ausbreitung der Bakterien wichtig sind.
Sporen an unerwarteter Stelle
„Wir haben das nicht erwartet, denn normalerweise bilden sich Sporen unter Stress, z.B. bei Austrocknung. Aber hier sind sie mit Wasserkanälen verbunden, wahrscheinlich durch die Anreicherung von Metallionen", sagt Chai.
Die Ergebnisse zeigen, dass die Strukturen in der Matrix nicht nur eine wichtige Rolle bei der Verteilung von Nährstoffen und Wasser spielen, sondern auch aktiv die Fähigkeit des Bakteriums beeinflussen, sich als mehrzelliger Organismus zu verhalten. „Dies könnte uns helfen, insgesamt mit Biofilmen besser zurecht zu kommen, sowohl mit den nützlichen als auch mit den schädlichen", sagt Liraz Chai.
Originalveröffentlichung
David N. Azulay, Oliver Spaeker, Mnar Ghrayeb, Michaela Wilsch-Braeuninger, Ernesto Scoppola, Manfred Burghammer, Ivo Zizak, Luca Bertinetti, Yael Politi and Liraz Chai: Multiscale X-ray study of Bacillus subtilis biofilms reveals interlinked structural hierarchy and elemental heterogeneity. PNAS (January 2022)
Link: https://doi.org/10.1073/pnas.2118107119
Über das B CUBE
Das B CUBE - Center for Molecular Bioengineering wurde 2008 als Zentrum für Innovationskompetenz (ZIK) durch die Initiative „Unternehmen Region“ des Bundesministeriums für Bildung und Forschung gegründet. Es ist Teil des Center for Molecular and Cellular Bioengineering (CMCB). Die Forschungstätigkeit des B CUBE konzentriert sich auf die Untersuchung lebender Strukturen auf molekularer Ebene und die Übersetzung der daraus resultierenden Erkenntnisse in innovative Methoden, Materialien und Technologien.
Web: www.tu-dresden.de/bcube
Weitere Informationen für Journalisten
Dr. Magdalena Gonciarz
Public Relations Officer
Center for Molecular and Cellular Bioengineering (CMCB)
E-mail:
Wissenschaftliche Ansprechpartner:
Prof. Yael Politi
Forschungsgruppenleiterin
B CUBE - Center for Molecular Bioengineering
E-mail:
