Research at the Chair of Special Food Chemistry
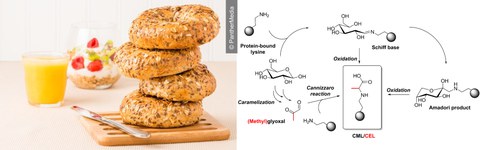
How does our body deal with the chemically modified amino acid N-ε-carboxymethyllysine (CML)?
N-ε-carboxymethyllysine is an amino acid formed in the Maillard reaction. It is ingested with our daily food but is not utilized by the body; instead, it enters the large intestine, where different microorganisms (the "intestinal microbiota") can metabolize the compound.
In the DFG project "Understanding the metabolism of N-ε-carboxymethyllysine in E. coli" we want to investigate the degradation of the amino acid in more detail in cooperation with the research group of PD Dr. Jürgen Lassak (LMU Munich).
Selection of publications on the topic:
Hellwig M, Auerbach C, Müller N, Samuel P, Kammann S, Beer F, Gunzer F, Henle T. Metabolization of the advanced glycation end product N-ε-carboxymethyllysine (CML) by different probiotic E. coli strains. J Agric Food Chem 2019, 67, 1963–1972. DOI: 10.1021/acs.jafc.8b06748
Graf von Armansperg B, Koller F, Gericke N, Hellwig M, Jagtap PKA, Heermann R, Hennig J, Henle T, Lassak J. Transcriptional regulation of the Nε-fructoselysine metabolism in Escherichia coli by global and substrate-specific cues. Mol Microbiol 2021, 115, 175–190. DOI: 10.1111/mmi.14608
Lassak J, Sieber A, Hellwig M. Exceptionally versatile take II: Post-translational modifications of lysine and their impact on bacterial physiology. Biol Chem 2022, 403, 819-858. DOI: 10.1515/hsz-2021-0382
Mehler J, Behringer KI, Rollins RE, Pisarz F, Klingl A, Henle T, Heermann R, Becker NS, Hellwig M, Lassak J. Identification of Pseudomonas asiatica subsp. bavariensis str. JM1 as the first Nε-carboxy(m)ethyllysine degrading soil bacterium. Environ Microbiol 2022, 24, 3229-3241. DOI: 10.1111/1462-2920.16079
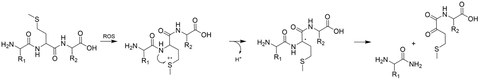
By which mechanisms are amino acids and peptides damaged in oxidation reactions?
Without oxygen, life on earth in its present form is not imaginable. And yet, oxygen adversely affects biomolecules. For proteins, this means that amino acid side-chains can be modified by reaction with reactive oxygen species. Moreover, degradation reactions can also occur in the peptide backbone. Methionine, for example, can promote α-amidation, probably by transferring oxidative damage from side-chain loci to the peptide backbone.
Selection of publications on the topic:
Hellwig M, Löbmann K, Orywol T: Peptide backbone cleavage by α-amidation is enhanced at methionine residues. J Pept Sci 2015, 21, 17-23. DOI: 10.1002/psc.2713
Hellwig M. The chemistry of protein oxidation in food. Angew Chem Int Ed 2019, 16742–16763. DOI: 10.1002/anie.201814144
Sajapin J, Hellwig M. Studies on the synthesis and stability of α-ketoacyl peptides. Amino Acids 2020, 52, 1425–1438. DOI: 10.1007/s00726-020-02902-8
Sajapin J, Kulas A, Hellwig M. Methionine-associated peptide α-amidation is directed both to the N- and the C-terminal amino acids. J Pept Sci 2022, 28, e3429. DOI: 10.1002/psc.3429
To what extent are dietary proteins subject to oxidation? How does this affect organoleptic properties?
When analyzing oxidative changes, special precautions are required, depending on the analyte, to avoid artificial formation of the target compounds. In addition, the informative value of some methods (e.g. protein carbonylation, AOPPs) is not yet definitively understood at the molecular level. Therefore, we are constantly optimizing our methods and adapting them to new questions.
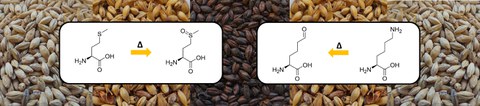
In malts, as the degree of browning increases, the free thiol groups and the amino acid methionine are degraded, forming methionine sulfoxide. Whether the oxidation of the malt proteins positively or negatively influences the oxidative stability of the malt and the beer produced from it must be clarified in further studies.
Selection of publications on the topic:
Kölpin M, Hellwig M. Quantitation of Methionine Sulfoxide in Milk and Milk-Based Beverages—Minimizing Artificial Oxidation by Anaerobic Enzymatic Hydrolysis. J Agric Food Chem 2019, 67, 8967-8976. DOI: 10.1021/acs.jafc.9b03605
Fleischer K, Hellwig M. Kilning invokes oxidative changes in malt proteins. Eur Food Res Technol 2023, 249, 199-206. DOI: 10.1007/s00217-022-04144-2
Sajapin J, Blümel B, Wichmann A, Gabel AK, Hellwig M. Stability of the glycated amino acid N-ε-(2-formyl-5-hydroxymethylpyrrol-1-yl)-L-norleucine (pyrraline) during oxidation. J Agric Food Chem 2024, 72, 24776-24785. DOI: 10.1021/acs.jafc.4c08539
How can alternative protein sources be used effectively in human nutrition?
The faba bean is a native legume that gradually disappeared from German culinary culture after the introduction of the potato and garden pea. The project investigates the composition of its nutrients and examines the reactivity of amino acids with other ingredients. Furthermore, new foods and food ingredients will be produced from the faba bean. The focus is on optimizing processing methods so that the nutritional value can be increased by reducing anti-nutritive substances.
This project is co-financed with funds from the European Union and co-financed with tax revenue based on the budget approved by the Saxon State Parliament.