Forschungsschwerpunkt
Bluthochdruck-bedingte Organschädigung - Pathophysiologie, Behandlung und geschlechtsspezifische Unterschiede
Chronisch erhöhter Blutdruck (Hypertonie) ist weltweit die Hauptursache für Morbidität und Mortalität. Derzeit sind weltweit mehr als eine Milliarde Menschen an Bluthochdruck erkrankt. Bluthochdruck führt letztlich zu einer Schädigung von Zielorganen wie Herz, Gefäßen, Nieren und Gehirn, wodurch sich das Risiko für Schlaganfall, Herzinfarkt, chronische Nierenerkrankungen und Demenz erhöht. Die derzeitige Behandlung konzentriert sich hauptsächlich auf die Senkung des arteriellen Blutdrucks, was nicht einer kausalen Therapie entspricht.
Unsere Forschung beinhaltet drei Hauptaspekte:
Metabolische Veränderungen in Endothelzellen und Adipozyten und deren Beitrag zur Organschädigung bei Bluthochdruck
Funktionsstörungen verschiedener Zellen tragen zum Organschaden bei Bluthochdruck bei, was die weitere Progression der Hypertonie fördert. Pathologische Veränderungen der homöostatischen Funktionen der Zellen und ihre Dysfunktion sind ohne metabolische Veränderungen in diesen Zellen nicht denkbar. Hier interessieren wir uns für den metabolischen Umbau der endothelialen und perivaskulären Adipozyten bei Bluthochdruck. Wir untersuchen insbesondere die Mechanismen, die zu diesen Stoffwechselveränderungen beitragen, und untersuchen ihre Bedeutung für die zelluläre Dysfunktion und die Organschäden bei Bluthochdruck.
Experimentelle inflammationshemmende Strategien für die Suche nach neuen Targets zur Behandlung der Organschädigung
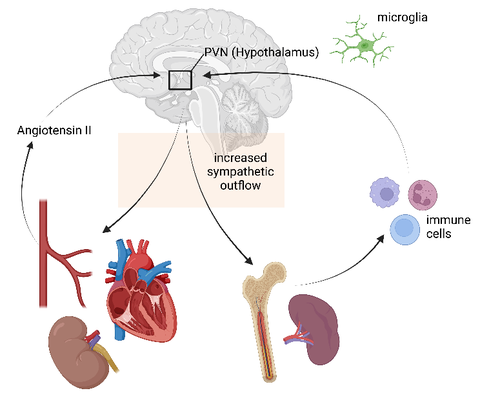
Abb. 1: Neuro-immune crosstalk und dessen Beitrag zu hypertensiven Organschäden. (biorender.com)
Es gibt deutliche Hinweise darauf, dass das Immunsystem eine ursächliche Rolle bei der Entstehung von Bluthochdruck und den damit verbundenen Zielorganschäden spielt. Ein komplexer neuro-immuner Crosstalk zwischen dem ZNS und peripheren Organen wie Milz und Knochenmark wurde in die Hypertonie einbezogen. So aktiviert beispielsweise ein verstärkter Sympathikotonus periphere Immunzellen, die zusammen mit blutdrucksteigernden Reizen wie Angiotensin II (ANGII) eine Mikroglia-Aktivierung und Neuroinflammation im Gehirn auslösen können. Aktivierte Mikroglia können dann die Sympathikusaktivität weiter steigern und so direkt Bluthochdruck und Organschäden beeinflussen. Daher erforschen wir Mechanismen der Immunmodulation, um neue Targets für die Hypertonietherapie zu finden.
Mechanismen der geschlechtsspezifischen Unterschiede bei Bluthochdruck und im Herz-Kreislaufsystem
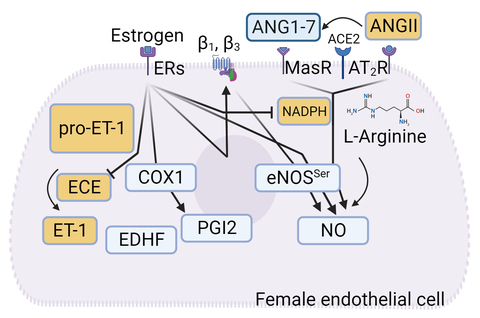
Abb. 2: Östrogen-abhängige Regulierung der β-Adrenozeptor-Expression und der Endothelfunktion.
Es gibt Geschlechtsunterschiede bei der Entwicklung von Bluthochdruck und damit verbundenen Organschäden. Während Frauen im Vergleich zu gleichaltrigen Männern später im Leben Bluthochdruck entwickeln, sind die Folgen kardiovaskulärer Komplikationen bei Frauen möglicherweise schlechter. Diese Unterschiede werden weitgehend auf Sexualhormone zurückgeführt. Wir untersuchen die geschlechtsabhängige Expression von endothelialen β1- und β3-Adrenozeptoren und ihre Rolle bei der Entwicklung von Bluthochdruck und Organschäden. Wir haben gezeigt, dass Östrogen, nicht aber andere Sexualhormone, die Expression dieser Adrenozeptoren regulieren. Daher untersuchen wir die Östrogenrezeptoren und die nachgeschaltete Signalkaskade bei der Regulierung der endothelialen β1- und β3-Adrenozeptoren.
Neben der hypertensiven Herzhypertrophie untersuchen wir auch die Mechanismen, die die kardiale Kontraktilität regulieren. Hier verwenden wir ein Mausmodell, bei dem sich kurz nach der Induktion eines Gen-Knockouts eine systolische Dysfunktion entwickelt. Diese Modelle kardialer Dysfunktion erfordern umfassende in vivo Untersuchungen der Herzfunktion. Mit Hilfe des Vevo3100 Bildgebungssystems von FUJIFILM VisualSonics sind wir in der Lage, Dimensionen von Herzstrukturen in unterschiedlichen Schnittbildern zu beurteilen, sowie systolische und diastolische Funktionsparameter zu bestimmen.
Abb. 3: Echokardiographie Mausherz.
Methoden:
- Implantation osmotischer Minipumpen (z.B. für kontinuierliche Angiotensin II-Infusion)
- Nicht-invasive Blutdruckmessung
- Histologie
- Immunfluoreszenz
- Mulvany Myographie
- RT-qPCR, Western blot
- Echokardiographie
- Durchflusszytometrie
- Metabolomics
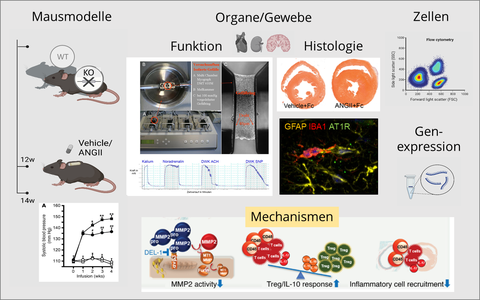
Abb. 4: Übersicht über Workflow und Methoden. DEL-1 Mechanismus siehe Failer T & Amponsah-Offeh, M et al. J Clin Invest. 2022;132(6):e126155 https://doi.org/10.1172/JCI126155 (biorender.com)
