KOMVITAL - Kontaktloses Monitoring von Vitaldaten
Unsere Vision
Für das Monitoring des Gesundheitszustandes im häuslichen Umfeld sind zahlreiche Gerätschaften notwendig. Patientinnen und Patienten neigen dazu, Messungen auszulassen, wenn diese besonders aufwändig sind.
KOMVITAL sieht die Lösung für dieses Problem im kontaktlosen Monitoring von Vitalparametern. Mit einer einfach zu bedienenden, intelligenten und vollintegrierten Messtechnik stößt KOMVITAL in die Zukunft des komfortablen, zuverlässigen häuslichen Gesundheitsmonitorings vor. Die Entwicklung entspringt dabei langjähriger forschungsgetriebener Expertise. Im Rahmen eines MDR Beitrags berichteten wir bereits über eine beispielhafte Umsetzung. Überzeugen Sie sich selbst:
Our contribution to MDR aktuell “Medicine of tomorrow”: Diagnosis from the mirror (English subtitles available). © Report from the ARD theme day “Medicine of tomorrow” from 09.04.2024 on MDR television.
Unsere Technologien
Kamerabasierte Photoplethysmographie erfordert ein komplexes Zusammenspiel aus Beleuchtungstechnik, Sensortechnik, Videoverarbeitung, Bildverarbeitung und Signalverarbeitung. Mit KOMVITAL werden die verschiedenen Teilbereiche zusammengeführt und in eine praxistaugliche Endanwendung gebracht. Um die Technologie nutzbar zu machen, stehen bei unserer Entwicklung folgende Aspekte im Vordergrund:
- innovative Algorithmik zur robusten Signalextraktion
von modellbasierten Verfahren über datengetriebene Empirie bis zur künstlichen Intelligenz - multimodale Messung kardiovaskulärer und respiratorischer Vitalparameter mit hoher Genauigkeit
von der Herztätigkeit über die Atmung bis zur Gefäßaktivität - explorative Messung in verschiedenen Umgebungen
vom intensivmedizinischen Monitoring in der Klinik über experimentelle Laboranordnungen bis zum vollintegrierten Prototypen im häuslichen Umfeld
Einen tieferen Einblick in unsere Technologien können Sie in den nachfolgenden Beiträgen erhalten:
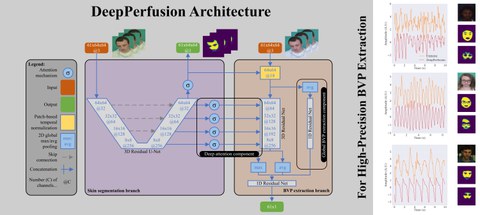
DeepPerfusion ist ein neuentwickelter Ansatz zur Extraktion der Blutvolumenpulsation auf Basis der kamerabasierten Photoplethysmographie. Der Einsatz einer speziell entwickelten künstlichen Intelligenz ermöglicht dabei eine signifikant präzisere Signalextraktion, wodurch die kamerabasierte Erfassung komplexerer Vitalparameter, wie beispielsweise des Blutdrucks, ermöglicht werden soll. Zudem ermöglicht DeepPerfusion den Signalursprung nachzuvollziehen und erlaubt folglich eine gewisse Erklärbarkeit. Die nachfolgende Abbildung gibt einen technischen Einblick in die Funktionsweise von DeepPerfusion und demonstriert die hohe Güte der extrahierten Signale. Die Veröffentlichung zu DeepPerfusion ist hier einsehbar.
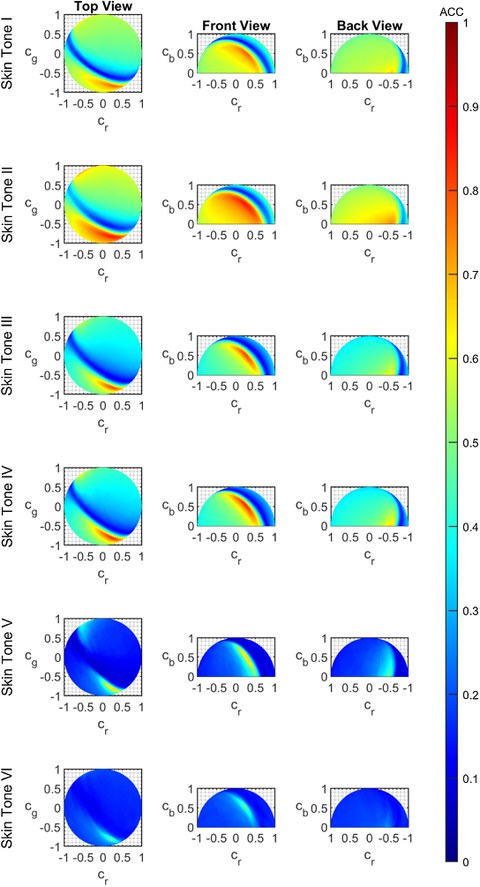
Mittels neu entwickelter Optimal Color Channel Combination (O3C) ist die Findung der optimalen Farbkanalkombination aus rotem, grünen und blauem Farbanteil in einem aufgenommenen RGB Video eines durchbluteten Hautareals möglich. Die optimale Linearkombination aus den einzelnen Farbanteilen verbessert dabei auf einfache Weise die Extraktion der Blutvolumenpulsation und eröffnet neue Möglichkeiten zur Signalauswertung. Die Veröffentlichung zu O3C ist hier einsehbar. Nachfolgend ist eine graphische Darstellung der O3C Ergebnisse aufgeführt.
Für die Anwendung der kamerabasierten Photoplethysmographie und die Extraktion der Blutvolumenpulsation ist üblicherweise die Detektion relevanter Hautareale notwendig. Hautareale welche beispielsweise behaart sind müssen ausgeschlossen werden. Dies sollte auch bei Bewegung robust funktionieren. Um diese Aufgabe bestmöglich zu erfüllen, wurde ein künstlisches neuronales Netz entwickelt und trainiert. Es konnte gezeigt werden, dass mit diesem Netzwerk die Haut robust und präzise detektiert werden kann und somit eine Verbesserung der Güte extrahierter Signale erreicht werden kann. Details zu diesem Ansatz sind hier einsehbar. Die nachfolgende Abbildung zeigt Ergebnisse dieses Ansatzes.
Nicht jede Messung liefert Signale mit ausreichender Qualität, z. B. im Fall von Bewegung (siehe Abbildung). Physiologische Informationen lassen sich aus Signalen mit unzureichender Qualität häufig nicht korrekt ableiten. Daher ist die automatisierte Bewertung der Signalqualität ein essentieller Bestandteil der Biosignalverarbeitung. Wir haben ein System entwickelt, dass diese Aufgabe ohne die Notwendigkeit von Referenzinformationen erfüllt. Die Veröffentlichung zur automatisierten Bewertung der Signalqualität ist hier einsehbar.
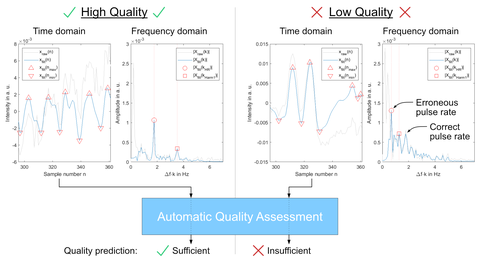
Principle of automatic quality assessment of cbPPG signals with a signal quality index filter.
Unser IP
Umfasst die Erfindung bezüglich der DeepPerfusion KI.
Umfasst die Erfindung zur kontaktlosen Blutdruckschätzung.
Unsere wissenschaftliche Expertise
Seit über 10 Jahren treibt das IBMT zahlreiche Entwicklungen auf dem Gebiet der kamerabasierten Photoplethysmographie voran. Nachfolgend sind einige ausgewählte Veröffentlichungen des IBMT auf dem Gebiet der kamerabasierten Photoplethysmographie gelistet:
M. Scherpf, H. Malberg, and M. Schmidt, "Improved Pulse Pressure Estimation Based on Imaging Photoplethysmographic Signals," in 2022 Computing in Cardiology Conference (CinC), 2022.
M. Scherpf, H. Ernst, H. Malberg, and M. Schmidt, "DeepPerfusion: Camera-based Blood Volume Pulse Extraction Using a 3D Convolutional Neural Network," in 2020 Computing in Cardiology, 2020, pp. 1–4. [Online]. Available: https://doi.org/10.22489/CinC.2020.388
H. Ernst, M. Scherpf, H. Malberg, and M. Schmidt, "Color Spaces and Regions of Interest in Camera Based Heart Rate Estimation," in 2020 11th Conference of the European Study Group on Cardiovascular Oscillations (ESGCO), Pisa, Italy, 72020, pp. 1–2.
A. Trumpp, "Remote Assessment of the Cardiovascular Function Using Camera-Based Photoplethysmography," Dissertation, Technische Universität Dresden, 2019. [Online]. Available: https://nbn-resolving.org/urn:nbn:de:bsz:14-qucosa2-367589
S. Zaunseder, A. Trumpp, H. Ernst, M. Förster, and H. Malberg, "Spatio-temporal analysis of blood perfusion by imaging photoplethysmography," in Optical Diagnostics and Sensing XVIII: Toward Point-of-Care Diagnostics: 29-30 January 2018, San Francisco, California, United States, San Francisco, United States, 2018, p. 32.
S. Zaunseder, A. Trumpp, D. Wedekind, and H. Malberg, "Cardiovascular assessment by imaging photoplethysmography - a review," Biomedizinische Technik. Biomedical engineering, vol. 63, no. 5, pp. 617–634, 2018.
A. Trumpp, P. L. Bauer, S. Rasche, H. Malberg, and S. Zaunseder, "The value of polarization in camera-based photoplethysmography," Biomedical optics express, vol. 8, no. 6, pp. 2822–2834, 2017, doi: 10.1364/BOE.8.002822.
A. Trumpp et al., "Skin Detection and Tracking for Camera-Based Photoplethysmography Using a Bayesian Classifier and Level Set Segmentation," in Bildverarbeitung für die Medizin, Heidelberg: Springer Vieweg, Berlin, Heidelberg, 2017, pp. 43–48. [Online]. Available: https://doi.org/10.1007/978-3-662-54345-0_16
D. Wedekind et al., "Assessment of blind source separation techniques for video-based cardiac pulse extraction," Journal of biomedical optics, vol. 22, no. 3, p. 35002, 2017, doi: 10.1117/1.JBO.22.3.035002.
A. Trumpp, J. Schell, H. Malberg, and S. Zaunseder, "Vasomotor assessment by camera-based photoplethysmography," Current Directions in Biomedical Engineering, vol. 2, no. 1, p. 21434, 2016, doi: 10.1515/cdbme-2016-0045.
F. Andreotti, A. Trumpp, H. Malberg, and S. Zaunseder, "Improved heart rate detection for camera-based photoplethysmography by means of Kalman filtering," in 2015 IEEE 35th International Conference on Electronics and Nanotechnology (ELNANO): 21 - 24 April 2015, Kyiv, Ukraine, Kyiv, Ukraine, 2015, pp. 428–433.
S. Zaunseder, A. Heinke, A. Trumpp, and H. Malberg, "Heart beat detection and analysis from videos," in 2014 IEEE 34th International Conference on Electronics and Nanotechnology (ELNANO): 15 - 18 April 2014, Kyiv, Ukraine, Kyiv, Ukraine, 2014, pp. 286–290.
H. Ernst, M. Scherpf, S. Pannasch, J. R. Helmert, H. Malberg, and M. Schmidt, "Assessment of the human response to acute mental stress-An overview and a multimodal study," PloS one, vol. 18, no. 11, e0294069, 2023, doi: 10.1371/journal.pone.0294069.
O. Bota et al., "Topical negative pressure wound therapy enhances the local tissue perfusion - A pilot study," Microvascular research, vol. 140, p. 104301, 2022, doi: 10.1016/j.mvr.2021.104301.
A. Hammer et al., "Camera-based assessment of cutaneous perfusion strength in a clinical setting," Physiological measurement, 2022, doi: 10.1088/1361-6579/ac557d.
S. Rasche et al., "Remote Photoplethysmographic Assessment of the Peripheral Circulation in Critical Care Patients Recovering From Cardiac Surgery," Shock (Augusta, Ga.), vol. 52, no. 2, pp. 174–182, 2019, doi: 10.1097/SHK.0000000000001249.
A. Trumpp et al., "Camera-based photoplethysmography in an intraoperative setting," Biomedical engineering online, vol. 17, no. 1, p. 33, 2018, doi: 10.1186/s12938-018-0467-7.
A. Trumpp et al., "Relation between pulse pressure and the pulsation strength in camera-based photoplethysmograms," Current Directions in Biomedical Engineering, vol. 3, no. 2, 2017, doi: 10.1515/cdbme-2017-0184.
Team

Doctoral Student | KOMVITAL
NameMr Dipl.-Ing. Matthieu Scherpf
Biosignal Processing Group
Send encrypted email via the SecureMail portal (for TUD external users only).
Visitor Address:
Fetscherforum (F29), 1st Floor, Room 32 Fetscherstr. 29
01307 Dresden
None

Postdoctoral Researcher | KOMVITAL
NameMr Dr.-Ing. Hannes Ernst-Völker
Biosignal Processing Group
Send encrypted email via the SecureMail portal (for TUD external users only).
Visiting address:
Fetscherforum (29), 1st Floor, Room 33 Fetscherstraße 29
01307 Dresden